计算题 适中0.65 引用1 组卷164
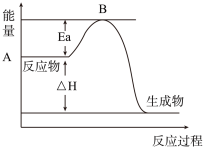
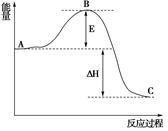
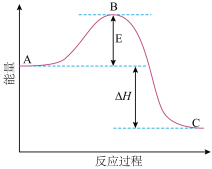
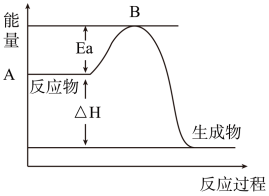
Ⅰ.2SO2(g)+O2(g)⇌2SO3(g)△H=a kJ•mol﹣1,反应过程的能量变化如图所示.已知1molSO2(g)完全转化为1molSO3(g)放热99kJ.请回答:
(1)a=__ kJ•mol﹣1.
(2)Ea的大小对该反应的△H___ (填“有”或“无”)影响.该反应常用V2O5作催化剂,加入V2O5会使图中B点__ (填“升高”、“降低”或“不变”).
(3)已知单质硫的燃烧热为296kJ•mol﹣1,写出反应的热化学方程式:____ .
Ⅱ.(1)工业上用H2和Cl2反应制HCl,各键能数据为:H﹣H:436kJ/mol,Cl﹣Cl:243kJ/mol,H﹣Cl:431kJ/mol.该反应的热化学方程式是______________ .
(2)由盖斯定律结合下述反应方程式,回答问题:
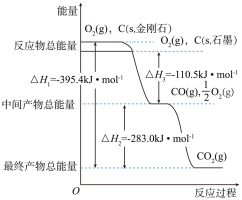
(1)已知:①C(s)+O2(g)=CO2(g) ΔH=ΔH1;
②2CO(g)+O2(g)=2CO2(g) ΔH=ΔH2;
③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=ΔH3;
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=________ 。(列出关于ΔH1、ΔH2、ΔH3的表达式)
(1)a=
(2)Ea的大小对该反应的△H
(3)已知单质硫的燃烧热为296kJ•mol﹣1,写出反应的热化学方程式:

Ⅱ.(1)工业上用H2和Cl2反应制HCl,各键能数据为:H﹣H:436kJ/mol,Cl﹣Cl:243kJ/mol,H﹣Cl:431kJ/mol.该反应的热化学方程式是
(2)由盖斯定律结合下述反应方程式,回答问题:
(1)已知:①C(s)+O2(g)=CO2(g) ΔH=ΔH1;
②2CO(g)+O2(g)=2CO2(g) ΔH=ΔH2;
③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=ΔH3;
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
20-21高二·宁夏银川·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网