解答题-工业流程题 较易0.85 引用1 组卷198
工业制硫酸的流程如图所示:
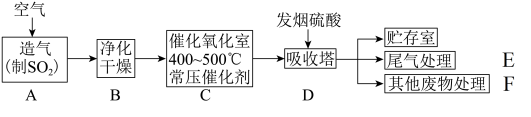
(1)早期以硫铁矿为原料造气,方程式为4FeS2+11O2 2Fe2O3+8SO2。若消耗了12gFeS2,上述反应有
2Fe2O3+8SO2。若消耗了12gFeS2,上述反应有___ mol电子发生了转移。
(2)如今大量改用固体硫为原料,同时生产过程中送入过量的空气,该改进从“减少污染物的排放”和___ 两个方面体现“绿色化学”。
(3)硫酸厂尾气处理的流程如图:
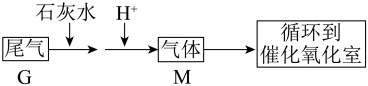
G的主要成分和M一样,如此处理的目的是___ ,将尾气G通入足量澄清石灰水,主要反应的离子方程式为___ 。
(4)如果C装置中生成0.1molSO3气体,可放出9.83kJ的热量。则该反应的热化学方程式为___ 。
(5)其他废弃物F中可能含有砷元素(As3+),处理工艺过程是在含砷废水中加入一定数量的硫酸亚铁,然后加碱调pH至8.5~9.0,反应温度90℃,鼓风氧化,废水中的砷、铁以砷酸铁(FeAsO4)沉淀析出,写出该过程的离子方程式___ 。

(1)早期以硫铁矿为原料造气,方程式为4FeS2+11O2
(2)如今大量改用固体硫为原料,同时生产过程中送入过量的空气,该改进从“减少污染物的排放”和
(3)硫酸厂尾气处理的流程如图:

G的主要成分和M一样,如此处理的目的是
(4)如果C装置中生成0.1molSO3气体,可放出9.83kJ的热量。则该反应的热化学方程式为
(5)其他废弃物F中可能含有砷元素(As3+),处理工艺过程是在含砷废水中加入一定数量的硫酸亚铁,然后加碱调pH至8.5~9.0,反应温度90℃,鼓风氧化,废水中的砷、铁以砷酸铁(FeAsO4)沉淀析出,写出该过程的离子方程式
20-21高三上·福建福州·开学考试
类题推荐
硫酸是一种重要的工业原料,工业制硫酸的流程如图所示。
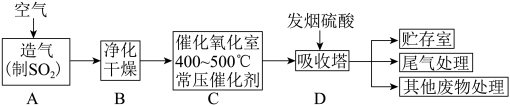
(1)早期以黄铁矿FeS2为原料造气,操作为在沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,其目的是_______ 。
(2)已知催化氧化室发生的反应2SO2+O2 2SO3为放热反应,下列有关说法错误的是_______。
2SO3为放热反应,下列有关说法错误的是_______。
(3)硫酸厂尾气处理的流程如图。
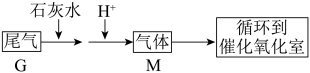
G的主要成分和M相同,足量石灰水吸收尾气产生的白色沉淀的化学式为_______ ,将气体M通入FeCl3溶液中,溶液最终变为浅绿色,反应的离子方程式为_______ 。
(4)其他废弃物中可能含有砷元素As3+,处理工艺过程是在含砷废水中加入一定数量的硫酸亚铁,然后加碱调pH至8.5~9.0,反应温度90 ℃,鼓风氧化,废水中的砷、铁以砷酸铁(FeAsO4)沉淀析出,写出该过程的离子方程式_______ 。

(1)早期以黄铁矿FeS2为原料造气,操作为在沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,其目的是
(2)已知催化氧化室发生的反应2SO2+O2
| A.使用催化剂是为了增大反应速率,提高生产效率 |
| B.提高反应时的温度,可以实现SO2的完全转化 |
| C.在上述条件下,SO2不可能100%地转化为SO3 |
| D.通过调控反应条件,可以提高反应进行的程度 |

G的主要成分和M相同,足量石灰水吸收尾气产生的白色沉淀的化学式为
(4)其他废弃物中可能含有砷元素As3+,处理工艺过程是在含砷废水中加入一定数量的硫酸亚铁,然后加碱调pH至8.5~9.0,反应温度90 ℃,鼓风氧化,废水中的砷、铁以砷酸铁(FeAsO4)沉淀析出,写出该过程的离子方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网