解答题-原理综合题 适中0.65 引用1 组卷166
25 ℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)CH3COOH、H2CO3、HClO 的酸性由强到弱的顺序为_____ 。
(2)同浓度的 CH3COO-、HCO 、CO
、CO 、ClO-结合 H+的能力由强到弱的顺序为
、ClO-结合 H+的能力由强到弱的顺序为_____ 。
(3)将少量 CO2 气体通入 NaClO 溶液中,写出反应的离子方程式:_____ 。
(4)常温下 0.1 mol·L-1 的 CH3COOH 溶液在加水稀释过程中,填写下列表达式中的数据 变化情况(填“变大”“变小”或“不变”)。
①
_____________________________________
②
_____________________________________
③
_____________________________________
| 化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)CH3COOH、H2CO3、HClO 的酸性由强到弱的顺序为
(2)同浓度的 CH3COO-、HCO
(3)将少量 CO2 气体通入 NaClO 溶液中,写出反应的离子方程式:
(4)常温下 0.1 mol·L-1 的 CH3COOH 溶液在加水稀释过程中,填写下列表达式中的数据 变化情况(填“变大”“变小”或“不变”)。
①
②
③
20-21高二上·甘肃兰州·期中
类题推荐
25℃时,部分物质的电离平衡常数如下表所示:
请回答下列问题。
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为___________ 。
(2)向0.1mol·L-1Na2CO3溶液中滴入酚酞溶液呈浅红色,其原因是___________ (用离子方程式表示),再将此溶液加热,溶液颜色___________ 。
(3)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:___________ 。
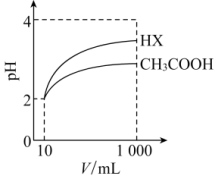
(4)10mLpH=2的醋酸与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___________ (填“大于”“等于”或“小于”)醋酸的电离平衡常数,理由是___________ 。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | 4.7×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为
(2)向0.1mol·L-1Na2CO3溶液中滴入酚酞溶液呈浅红色,其原因是
(3)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:
(4)10mLpH=2的醋酸与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数

25 ℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为___________ 。
(2)同浓度的CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为_________________ 。
(3)物质的量浓度均为0.1 mol·L-1的下列四种物质的溶液:a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3,pH由大到小的顺序是______ (填编号)。
(4)体积为10 mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000 mL,稀释过程中pH变化如图所示,

则HX的电离平衡常数____ (填“大于”、“等于”或“小于”)醋酸的电离平衡常数;理由是___________________ 。稀释后,HX溶液中由水电离出来的c(H+)_______ (填“大于”、“等于”或“小于”)
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为
(2)同浓度的CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为
(3)物质的量浓度均为0.1 mol·L-1的下列四种物质的溶液:a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3,pH由大到小的顺序是
(4)体积为10 mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000 mL,稀释过程中pH变化如图所示,

则HX的电离平衡常数
请回答下列问题:
(1)某温度时,测得pH=11的Ba(OH)2溶液浓度是0.005 mol·L-1。
①该温度下水的离子积常数Kw=_______ 。
②在此温度下,将pH=12的Ba(OH)2溶液与pH=2的硫酸溶液等体积混合,所得混合液呈_______ 性(填“酸”,“碱”或“中”)。
(2)25 ℃时,部分物质的电离平衡常数如表所示。请回答下列问题:
①下列说法正确的是_______ 。
A.25 ℃时,向CH3COOH溶液中加入适量的NaOH溶液,CH3COOH的电离程度增大,电离平衡常数不变
B.0.1 mol·L-1 CH3COOH溶液加水稀释,稀释后的溶液中水的电离程度减小
C.0.1 mol·L-1 HClO溶液和0.1 mol·L-1 NaClO溶液等体积混合溶液呈碱性
D.碳酸氢钠溶液中阴、阳离子数目相等
②同浓度的CH3COO-、HCO 、CO
、CO 、ClO-结合H+的能力由强到弱顺序为
、ClO-结合H+的能力由强到弱顺序为_______ 。
③25 ℃时,某CH3COOH和CH3COOK混合溶液呈中性,则该混合溶液中: =
=_______ 。
(3)25 ℃时,HF的Ka=6.4×10-4 则此温度下0.1 mol·L-1 HF溶液的c(H+)为_______ mol·L-1。
(1)某温度时,测得pH=11的Ba(OH)2溶液浓度是0.005 mol·L-1。
①该温度下水的离子积常数Kw=
②在此温度下,将pH=12的Ba(OH)2溶液与pH=2的硫酸溶液等体积混合,所得混合液呈
(2)25 ℃时,部分物质的电离平衡常数如表所示。请回答下列问题:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
A.25 ℃时,向CH3COOH溶液中加入适量的NaOH溶液,CH3COOH的电离程度增大,电离平衡常数不变
B.0.1 mol·L-1 CH3COOH溶液加水稀释,稀释后的溶液中水的电离程度减小
C.0.1 mol·L-1 HClO溶液和0.1 mol·L-1 NaClO溶液等体积混合溶液呈碱性
D.碳酸氢钠溶液中阴、阳离子数目相等
②同浓度的CH3COO-、HCO
③25 ℃时,某CH3COOH和CH3COOK混合溶液呈中性,则该混合溶液中:
(3)25 ℃时,HF的Ka=6.4×10-4 则此温度下0.1 mol·L-1 HF溶液的c(H+)为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


