填空题 适中0.65 引用3 组卷171
工业上可用H2和CO2制备甲醇,其反应方程式为CO2(g)+3H2(g) CH3OH(g)+H2O(g),某温度下,将1 mol CO2和3 mol H2充入体积不变的2 L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
CH3OH(g)+H2O(g),某温度下,将1 mol CO2和3 mol H2充入体积不变的2 L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
(1)用H2表示前2 h 的平均反应速率v(H2)=__________________________ ;
(2)该温度下,CO2的平衡转化率为________ 。
(3)在温度为T,压强为P的条件下,将CO2和H2按物质的量之比1∶3 通入一恒压密闭容器中发生上述反应,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数为Kp=________ (用含P的表达式表示,其中用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
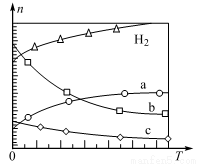
(4)CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g) C2H4(g)+4H2O(g) ΔH。在0.1 MPa时,按n(CO2)∶n(H2)=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
C2H4(g)+4H2O(g) ΔH。在0.1 MPa时,按n(CO2)∶n(H2)=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
①该反应的ΔH________ 0(填“>”或“<”)。
②曲线c表示的物质为________ 。
③为提高H2的平衡转化率,除改变温度外,还可采取的措施是______________ 。(答出一条即可)
时间/h | 1 | 2 | 3 | 4 | 5 | 6 |
0.90 | 0.85 | 0.83 | 0.81 | 0.80 | 0.80 |
(2)该温度下,CO2的平衡转化率为
(3)在温度为T,压强为P的条件下,将CO2和H2按物质的量之比1∶3 通入一恒压密闭容器中发生上述反应,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数为Kp=
(4)CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g)

①该反应的ΔH
②曲线c表示的物质为
③为提高H2的平衡转化率,除改变温度外,还可采取的措施是
20-21高二上·湖北襄阳·期中
类题推荐
回答下列问题:
(1)工业上可用 与
与 制备甲醇,其反应的化学方程式为
制备甲醇,其反应的化学方程式为 。某温度下,将
。某温度下,将 与
与 充入容积不变的
充入容积不变的 密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
①用 表示前
表示前 的平均反应速率
的平均反应速率
_______ 。
②该温度下, 的平衡转化率为
的平衡转化率为_______ 。
③在300℃、 下,将
下,将 与
与 按物质的量之比
按物质的量之比 通入一密闭容器中发生上述反应达到平衡时,测得
通入一密闭容器中发生上述反应达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数为
的平衡转化率为50%,则该反应条件下的平衡常数为
_______ (结果保留二位有效数字)。
(2) 经催化加氢可合成低碳烯烃:
经催化加氢可合成低碳烯烃:
 。在
。在 时,按
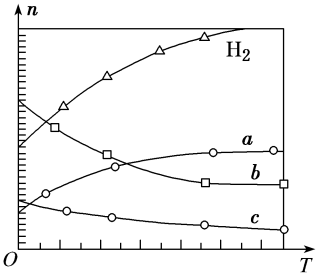
时,按 投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
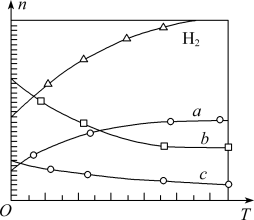
②该反应的
_______ (填“>”或“<”)0。
③曲线c表示的物质为_______ 。(填写化学式)
④在不改变起始投料的前提下,为提高 的平衡转化率,除改变温度外,还可采取的措施是
的平衡转化率,除改变温度外,还可采取的措施是_______ 。(任写一项措施)
(1)工业上可用
| 时间/h | 1 | 2 | 3 | 4 | 5 | 6 |
| 0.90 | 0.85 | 0.83 | 0.81 | 0.80 | 0.80 |
②该温度下,
③在300℃、
(2)

②该反应的
③曲线c表示的物质为
④在不改变起始投料的前提下,为提高
对 的资源化利用可以获得重要的化工产品和燃料,回答下列问题:
的资源化利用可以获得重要的化工产品和燃料,回答下列问题:
(1)已知①

②

写出 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为_______ 。
(2) 经催化加氢可合成烯烃:
经催化加氢可合成烯烃:
 ,在0.1MPa时,按
,在0.1MPa时,按 投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
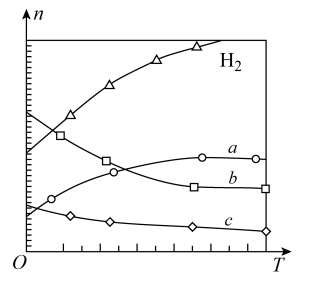
①该反应的
_______ 0(填“>”或“<”)。
②曲线c表示的物质为_______ (用化学式表示)。
③为提高 的平衡转化率,除改变温度外,还可采取的措施
的平衡转化率,除改变温度外,还可采取的措施_______ (答出一条即可)。
(3) 和
和 制备甲醇反应方程式
制备甲醇反应方程式
 ,某温度下,将
,某温度下,将 和
和 充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如下表:
充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如下表:
①用 表示前2h的平均反应速率
表示前2h的平均反应速率
_______  。
。
②该条件下的分压平衡常数为
_______  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③若该条件下 ,
, ,其中
,其中 、
、 为仅与温度有关的速率常数,
为仅与温度有关的速率常数,
_______ (填数值);若将温度升高,则反应速率增大的倍数;
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(1)已知①
②
写出
(2)

①该反应的
②曲线c表示的物质为
③为提高
(3)
| 时间/h | 1 | 2 | 3 | 4 | 5 |
| 0.92 | 0.85 | 0.79 | 0.75 | 0.75 |
②该条件下的分压平衡常数为
③若该条件下
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
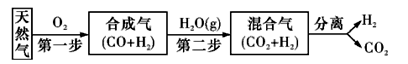
 2CO(g)+4H2(g)的△H=
2CO(g)+4H2(g)的△H= CH3OH(g)+ H2O(g)。某温度下,将1 mol CO2和3 mol H2充人体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表所示:
CH3OH(g)+ H2O(g)。某温度下,将1 mol CO2和3 mol H2充人体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表所示: