解答题-无机推断题 适中0.65 引用1 组卷110
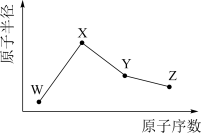
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大。
(1)X位于元素周期表中的位置为____________ W的基态原子核外有________ 个未成对电子。
(2)Z的气态氢化物和溴化氢相比,较稳定的是(写化学式)______ 。沸点较高的是(写化学式)___ 。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是_______________ 。

(1)X位于元素周期表中的位置为
(2)Z的气态氢化物和溴化氢相比,较稳定的是(写化学式)
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是
19-20高二下·江苏盐城·阶段练习
类题推荐
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大。

Ⅰ.(1)X位于元素周期表中的位置______________ ;W的基态原子核外有_________ 个未成对电子。
(2)X的单质和Y的单质相比,熔点较高的是__________ (写化学式);Z的气态氢化物和溴化氢相比,较稳定的是___________ (写化学式)。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是____________ 。
Ⅱ.部分化学键的键能见下表:
(1)比较下列两组物质的熔点高低(填“”“”)SiC________ Si;SiCl4________ SiO2
(2)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) Si(s)+4HCl(g),
Si(s)+4HCl(g),
计算该反应的反应热△H=_________ kJ·mol-1。

Ⅰ.(1)X位于元素周期表中的位置
(2)X的单质和Y的单质相比,熔点较高的是
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是
Ⅱ.部分化学键的键能见下表:
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/ kJ•mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
(2)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)
 Si(s)+4HCl(g),
Si(s)+4HCl(g),计算该反应的反应热△H=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网




