解答题-工业流程题 适中0.65 引用1 组卷79
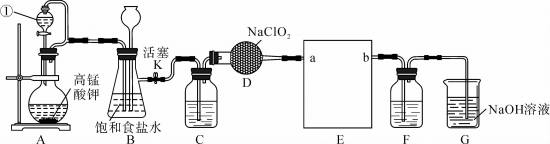
某同学取海带灰加蒸馏水煮沸 ,冷却,过滤,获得含I-的溶液,并设计如图所示实验方案,从中提取I2。
,冷却,过滤,获得含I-的溶液,并设计如图所示实验方案,从中提取I2。
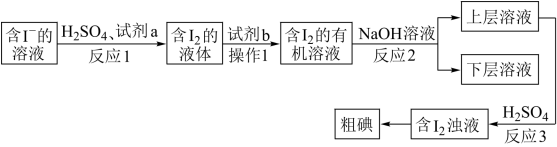
(1)反应1中硫酸的作用是提供酸性环境,则试剂a的作用是__________ 。
(2)试剂b应选择____________ (填标号)。
A.CCl4 B.酒精 C.醋酸
(3)操作1的名称是_________ 。实验室里进行操作1需要的玻璃仪器除烧杯外,还需要______ 。
(4)反应2为3I2+6NaOH=5NaI+NaIO3+3H2O。此反应的氧化剂是____________ ,氧化产物是____________ 。
(5)反应3的化学方程式是____________ 。

(1)反应1中硫酸的作用是提供酸性环境,则试剂a的作用是
(2)试剂b应选择
A.CCl4 B.酒精 C.醋酸
(3)操作1的名称是
(4)反应2为3I2+6NaOH=5NaI+NaIO3+3H2O。此反应的氧化剂是
(5)反应3的化学方程式是
19-20高一·全国·课时练习
类题推荐  是一种重要的氧化剂、杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
是一种重要的氧化剂、杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:

(1) 中Cl的化合价为
中Cl的化合价为_______ ,氯在元素周期表中的位置_______ 。
(2)写出“反应”步骤中生成 的化学方程式
的化学方程式_______ ,并标出电子转移的方向和数目。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 和
和 ,要加入的试剂分别为
,要加入的试剂分别为_______ 、_______ 。
(4)“电解”中阴极反应的主要产物是 ,写出阴板区的电极反应方程式
,写出阴板区的电极反应方程式_______ 。
(5)“尾气吸收”是吸收“电解”过程排出的少量 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为_______ ,该反应中氧化产物是_______ 。
(6)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为_______ (计算结果保留两位小数)。
(7) 溶液作为吸收剂可同时对烟气进行脱硫、脱硝,在反应器中通入含有
溶液作为吸收剂可同时对烟气进行脱硫、脱硝,在反应器中通入含有 和NO的烟气,一段时间后溶液中离子浓度的分析结果如下表:
和NO的烟气,一段时间后溶液中离子浓度的分析结果如下表:
①出实验结果可知,脱硫反应速率_______ 脱硝反应速率。
A.大于B.小于
②原因是除了 和NO在烟气中的初始浓度不同,还可能是
和NO在烟气中的初始浓度不同,还可能是_______ (写出一点即可)。
镁合金及镁的化合物在生产、生活中有着广泛的应用。
(1)镁在元素周期表中的位置是__________________ 。
(2)用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁的关键流程如下:

该工艺中可循环使用的物质有______________ 。
(3)储氢材料Mg(AlH4)2在110~200 ℃的反应为Mg(AlH4)2=MgH2+2Al+3H2↑,每转移6 mol电子生成氢气的物质的量为________ mol。
(4)碱式碳酸镁密度小,是橡胶制品的优良填料,可用复盐MgCO3·(NH4)2CO3·2H2O作原料制备。制备过程中,需要用到卤水(氯化镁溶液)。某科研小组用沉淀滴定法分析产品中Cl-的含量,称取6.1000 g产品用适量硝酸溶解,经稀释等步骤最终配得500 mL的溶液。
a.准确量取25.00 mL 待测液,用0.100 0 mol/L AgNO3标准液滴定,滴定前后滴定管中的液面读数如图所示,则滴定过程中消耗标准液的体积为________ mL。

b.
参照上表数据及信息分析,滴定时可以作指示剂的是________ (填数字序号)。
①CaCl2 ②NaBr ③NaI ④K2CrO4
(1)镁在元素周期表中的位置是
(2)用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁的关键流程如下:

该工艺中可循环使用的物质有
(3)储氢材料Mg(AlH4)2在110~200 ℃的反应为Mg(AlH4)2=MgH2+2Al+3H2↑,每转移6 mol电子生成氢气的物质的量为
(4)碱式碳酸镁密度小,是橡胶制品的优良填料,可用复盐MgCO3·(NH4)2CO3·2H2O作原料制备。制备过程中,需要用到卤水(氯化镁溶液)。某科研小组用沉淀滴定法分析产品中Cl-的含量,称取6.1000 g产品用适量硝酸溶解,经稀释等步骤最终配得500 mL的溶液。
a.准确量取25.00 mL 待测液,用0.100 0 mol/L AgNO3标准液滴定,滴定前后滴定管中的液面读数如图所示,则滴定过程中消耗标准液的体积为

b.
| AgCl | AgBr | AgI | Ag2CrO4 | |
| Ksp | 2×10-10 | 5.4×10-13 | 8.3×10-17 | 2×10-12 |
| 颜色 | 白 | 淡黄 | 黄 | 砖红 |
①CaCl2 ②NaBr ③NaI ④K2CrO4

(1)
(2)写出“反应”步骤中生成
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去
(4)“电解”中阴极反应的主要产物是
(5)“尾气吸收”是吸收“电解”过程排出的少量
(6)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
(7)
| 离子 | |||||
A.大于B.小于
②原因是除了
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网