填空题 适中0.65 引用2 组卷65
为了除去粗盐(主要成分为NaCl)样品中含有的少量氯化钙、氯化镁和硫酸钠杂质,某同学运用所学知识设计了如图所示的除杂方案。
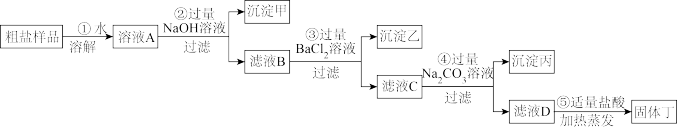
请根据上述除杂方案,回答下列问题:
(1)沉淀甲的主要成分是____________ (填化学式,后同);沉淀乙是______ ;沉淀丙是______ ;滤液C中的溶质是__________ ;⑤中加入适量盐酸的目的是______________________ 。
(2)假设整个操作过程中物质转化无损失,则固体丁中NaCl的质量相对于样品中NaCl的质量是____ (填“增大”“不变”或“减小”)的;若在②中改为加入过量的KOH溶液,则固体丁中可能含有的杂质是______ 。

请根据上述除杂方案,回答下列问题:
(1)沉淀甲的主要成分是
(2)假设整个操作过程中物质转化无损失,则固体丁中NaCl的质量相对于样品中NaCl的质量是
19-20高一·全国·课时练习
类题推荐
回答下列问题
(1)实验室配制FeSO4溶液时为防止硫酸亚铁变质,常采用的措施是___________ (填一种)。
(2)以FeSO4为原料可制备碱式硫酸铁[Fe4(OH)2(SO4)5]、X、硫酸亚铁铵[(NH4)2Fe(SO4)2,俗名摩尔盐],转化关系如图1所示。
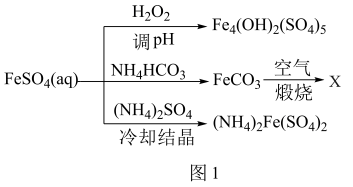
①制备Fe4(OH)2(SO4)5时,若pH过高会导致碱式硫酸铁的产率偏低,其原因是___________ 。
②制备FeCO3时,向FeSO4溶液中加入过量的NH4HCO3溶液,该反应的离子方程式为___________ ;X的化学式为___________ 。
③制备摩尔盐时将反应物混合,经蒸发浓缩、冷却结晶、___________ 、洗涤、干燥得到产品。
(3)隔绝空气条件下,FeSO4分解时的物质转化关系如图2。

①关于M的成分提出三种猜想:
猜想1:M是Fe2O3;
猜想2:M是___________ ;
猜想3:M是Fe2O3和Fe3O4。
②已知三种气体的部分性质如表所示:
利用图3装置探究硫酸亚铁部分分解产物。能否将低温浴槽A的温度控制在-72.4℃<T≤44.8℃?___________ (填“能”或“否”)。C中试剂可能是___________ 。

(1)实验室配制FeSO4溶液时为防止硫酸亚铁变质,常采用的措施是
(2)以FeSO4为原料可制备碱式硫酸铁[Fe4(OH)2(SO4)5]、X、硫酸亚铁铵[(NH4)2Fe(SO4)2,俗名摩尔盐],转化关系如图1所示。

①制备Fe4(OH)2(SO4)5时,若pH过高会导致碱式硫酸铁的产率偏低,其原因是
②制备FeCO3时,向FeSO4溶液中加入过量的NH4HCO3溶液,该反应的离子方程式为
③制备摩尔盐时将反应物混合,经蒸发浓缩、冷却结晶、
(3)隔绝空气条件下,FeSO4分解时的物质转化关系如图2。

①关于M的成分提出三种猜想:
猜想1:M是Fe2O3;
猜想2:M是
猜想3:M是Fe2O3和Fe3O4。
②已知三种气体的部分性质如表所示:
| 物质 | SO3 | SO2 | N2 |
| 熔点/℃ | 16.8 | -72.4 | -210 |
| 沸点/℃ | 44.8 | -10 | -195.8 |

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网