单选题 较易0.85 引用2 组卷170
某浓度的HF溶液中存在平衡:HF H++F-,若要增大F-的浓度,同时减小H+的浓度,可以采取的方法是( )
H++F-,若要增大F-的浓度,同时减小H+的浓度,可以采取的方法是( )
 H++F-,若要增大F-的浓度,同时减小H+的浓度,可以采取的方法是( )
H++F-,若要增大F-的浓度,同时减小H+的浓度,可以采取的方法是( )| A.加入少量NaOH固体 | B.适当降低温度 |
| C.加入少量的浓盐酸 | D.加水稀释 |
20-21高二上·河北邢台·期中
类题推荐
常温下,将0.1  NaOH滴到0.1
NaOH滴到0.1
 溶液中,混合溶液的pH与离子浓度变化关系如图所示,下列叙述不正确的是
溶液中,混合溶液的pH与离子浓度变化关系如图所示,下列叙述不正确的是
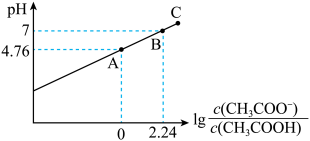

| A.常温下,醋酸的电离平衡常数 |
| B.在 |
| C.C点的溶质可能为 |
| D.当0.1 |
25℃,相同pH、相同体积的盐酸和醋酸溶液分别加水稀释,pH随溶液体积的变化如图所示。下列判断正确的是
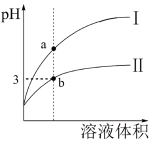

| A.Ⅰ为醋酸稀释时的pH变化 | B.未稀释时两溶液的导电能力不同 |
| C.b点水电离的c(H+)=1×10-11mol/L | D.a、b两点酸溶液的浓度相同 |
下列说法正确的是
| A.25℃时,向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| B.25℃时,某物质的溶液pH < 7,则该物质一定是酸或强酸弱碱盐 |
| C.25℃时,稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小 |
| D.常温下,在1L0.1mol•L-1醋酸溶液,加入少量CH3COONa固体后,溶液的pH降低 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


