解答题-原理综合题 适中0.65 引用2 组卷113
一种利用含硫物质的热化学循环来实现能量的转化与存储的构想如图所示:
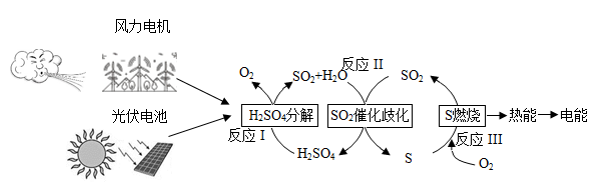
回答下列问题:
(1)举出图中两种形式的能量转化:________ 、________ 。
(2)反应I的化学方程式为_________ 。
(3)研究表明,I-可以作为水溶液中SO2歧化反应的催化剂,催化过程如下:
i.________ (请补充完整);
ii. I2+2H2O+SO2=4H++SO +2I-。
+2I-。
(4)SO2歧化反应速率与i、ii反应速率有一定关系,某同学设计实验如下:分别将18 mL SO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象。
已知:I2易溶解在KI溶液中。
①B是A的对比实验,a=_______ ;A、B对比实验说明________ ;A、C对比实验说明________ 。
②实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:________ 。
(5)已知原子利用率是指目标产物中某原子的总质量与反应物中某原子的总质量之比。反应Ⅱ若目标产物是H2SO4,则硫原子利用率为________ %(结果保留三位有效数字)。

回答下列问题:
(1)举出图中两种形式的能量转化:
(2)反应I的化学方程式为
(3)研究表明,I-可以作为水溶液中SO2歧化反应的催化剂,催化过程如下:
i.
ii. I2+2H2O+SO2=4H++SO
(4)SO2歧化反应速率与i、ii反应速率有一定关系,某同学设计实验如下:分别将18 mL SO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象。
| 序号 | A | B | C | D |
| 试剂组成 | 0.4 mol•L-1的KI | a mol•L-1的KI 0.2 mol•L-1的H2SO4混合物 | 0.2 mol•L-1的H2SO4 | 0.2 mol•L-1的KI和0.0002 mol I2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
①B是A的对比实验,a=
②实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:
(5)已知原子利用率是指目标产物中某原子的总质量与反应物中某原子的总质量之比。反应Ⅱ若目标产物是H2SO4,则硫原子利用率为
20-21高三上·湖南·阶段练习
类题推荐
近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如图:
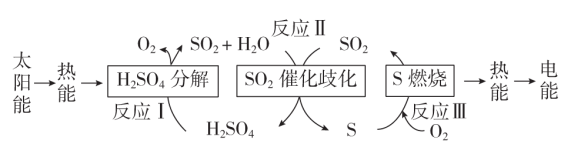
(1)反应I:2H2SO4(l)= 2SO2(g) +2H2O(g)+O2(g) ∆H1=+551 kJ ·mol-1
反应III:S(s)+O2(g)=SO2(g) ∆H3= -297 kJ·mol-1
反应II的热化学方程式:_______ 。
(2)对反应II,在一某投料比时,两种压强下 ,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示, p1_______ p2(填“>”或“< ”)。

(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下,将ii补充完整。
i.SO2+4I- +4H+ =S↓+2I2+2 H2O
ii.I2 +2H2O+SO2=_______ +2I-
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如表:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象,(已知:I2易溶解在KI溶液中)
①B是A的对比实验,则a=_______ 。
②比较A、B、C,可得出的结论是_______ 。
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:_______ 。

(1)反应I:2H2SO4(l)= 2SO2(g) +2H2O(g)+O2(g) ∆H1=+551 kJ ·mol-1
反应III:S(s)+O2(g)=SO2(g) ∆H3= -297 kJ·mol-1
反应II的热化学方程式:
(2)对反应II,在一某投料比时,两种压强下 ,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示, p1

(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下,将ii补充完整。
i.SO2+4I- +4H+ =S↓+2I2+2 H2O
ii.I2 +2H2O+SO2=
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如表:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象,(已知:I2易溶解在KI溶液中)
| 序号 | A | B | C | D |
| 试剂组成 | 0.2 mol·L-1 KI | amol·L-1 KI 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 KI 0.0002mol I2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
①B是A的对比实验,则a=
②比较A、B、C,可得出的结论是
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:
近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如图:
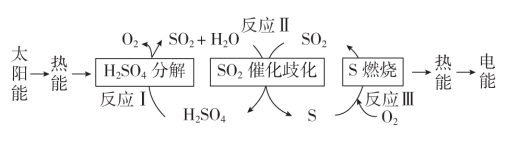
(1)反应Ⅱ:3SO2(g)+2H2O(g)=2H2SO4(l)+S(s) ΔH=-254 kJ·mol-1;对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。
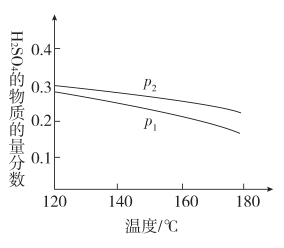
p2_______ p1(填“>”或“<”),得出该结论的理由是_______ 。
(2)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ⅱ补充完整。
ⅰ.SO2+4I-+4H+=S↓+2I2+2H2O
ⅱ.I2+2H2O+_______ =_______ +_______ +2I-
(3)探究ⅰ、ⅱ反应速率与SO2歧化反应速率的关系,实验如表:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
①B是A的对比实验,则a=_______ 。
②比较A、B、C,可得出的结论是_______ 。
③实验表明,SO2的歧化反应速率D>A,结合ⅰ、ⅱ反应速率解释原因:_______ 。

(1)反应Ⅱ:3SO2(g)+2H2O(g)=2H2SO4(l)+S(s) ΔH=-254 kJ·mol-1;对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。

p2
(2)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ⅱ补充完整。
ⅰ.SO2+4I-+4H+=S↓+2I2+2H2O
ⅱ.I2+2H2O+
(3)探究ⅰ、ⅱ反应速率与SO2歧化反应速率的关系,实验如表:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
| 序号 | A | B | C | D |
| 试剂组成 | 0.4 mol·L-1 KI | a mol·L-1 KI,0.2mol·L-1 H2SO4 | 0.2mol·L-1H2SO4 | 0.2 mol·L-1 KI,0.0002 mol I2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
①B是A的对比实验,则a=
②比较A、B、C,可得出的结论是
③实验表明,SO2的歧化反应速率D>A,结合ⅰ、ⅱ反应速率解释原因:
近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
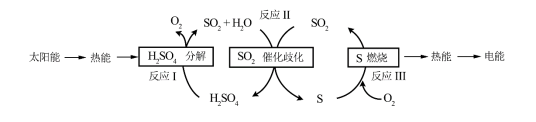
(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式:________________________________ 。
(2)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+_________=_________+_______+2 I-_____________
(3)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
①B是A的对比实验,则a=__________ 。
②比较A、B、C,可得出的结论是______________________ 。
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:________________ 。

(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式:
(2)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+_________=_________+_______+2 I-
(3)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
| 序号 | A | B | C | D |
| 试剂组成 | 0.4 mol·L-1 KI | a mol·L-1 KI 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 KI 0.0002 mol I2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
①B是A的对比实验,则a=
②比较A、B、C,可得出的结论是
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


