填空题 适中0.65 引用2 组卷27
下下列反应均可用于实验室制备氯气:
①MnO2+4HCl (浓) MnCl2+2H2O+Cl2↑。
MnCl2+2H2O+Cl2↑。
②KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
回答下列问题:
(1)请将反应①改写为离子方程式:____________ 。
(2)用双线桥标出反应②的电子转移方向和数目:__________ 。
(3)用单线桥标出反应③的电子转移方向和数目:___________
(4)比较反应①②中氧化剂的氧化性强弱____________ 。
(5)上述反应中浓盐酸显示出来的性质是_________ (填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(6)若反应①中有17.4 g纯MnO2被还原,则反应①中被氧化的氯化氢的质量为______ 。
(7)当反应①中生成3.01×1023个氯气分子时,则转移的电子数为_____ 。
(8)工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式__________ ,其反应中被氧化的原子与被还原的原子个数之比为_____ 。
①MnO2+4HCl (浓)
②KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
回答下列问题:
(1)请将反应①改写为离子方程式:
(2)用双线桥标出反应②的电子转移方向和数目:
(3)用单线桥标出反应③的电子转移方向和数目:
(4)比较反应①②中氧化剂的氧化性强弱
(5)上述反应中浓盐酸显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(6)若反应①中有17.4 g纯MnO2被还原,则反应①中被氧化的氯化氢的质量为
(7)当反应①中生成3.01×1023个氯气分子时,则转移的电子数为
(8)工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式
19-20高一·浙江·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
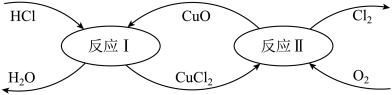
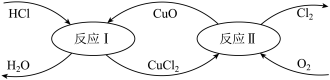
 2KCl+2MnCl2+5Cl2↑+8H2O
2KCl+2MnCl2+5Cl2↑+8H2O  Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
Cu(NO3)2+2NO2↑+2H2O,回答下列问题:

