单选题 适中0.65 引用3 组卷322
用相同的铝片、6 mol·L-1稀盐酸、3 mol·L-1稀硫酸、6 mol·L-1氢氧化钠溶液、试管等分别进行下表实验:
对上述实验的相关说法不正确 的是
| 实验方案 | 实验现象 | 实验原理(化学方程式) |
| (1)铝片与足量盐酸反应 | 铝片开始无现象,一段时间后逐渐溶解,并有大量气泡产生 | Al2O3+6HCl=2AlCl3+3H2O 2Al+6HCl=2AlCl3+3H2↑ |
| (2)铝片与足量硫酸反应 | 铝片开始无现象,一段时间后反应缓慢,铝片表面有少量气泡产生 | Al2O3+3H2SO4=2Al2(SO4)3+3H2O 2Al+3H2SO4=2Al2(SO4)3+3H2↑ |
| (3)铝片与足量氢氧化钠溶液反应 | 铝片开始无现象,一段时间后铝片逐渐溶解,并有大量气泡产生 | Al2O3+2NaOH=2NaAlO2+H2O 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ |
| A.对比(1)、(2)、(3)中Al2O3参与的反应可得出:Al2O3既有碱性氧化物的某些性质,又有酸性氧化物的某些性质 |
| B.对比(1)、(2)、(3)中气体产生现象和酸碱的挥发性可得出:实验(3)最适宜于实验室制备H2 |
| C.对比实验(1)、(2)中后来产生气泡的现象,可得出:c(H+)越大,相同时间内产生气泡越多 |
| D.对比实验(1)、(2)中后来产生气泡的现象,可得出: |
20-21高一上·江苏徐州·阶段练习
类题推荐
用相同的铝片、6mol/L稀盐酸、3mol/L稀硫酸、6mol/L氢氧化钠溶液分别进行以下实验:
对上述实验的相关说法不正确的是
| 实验方案 | 实验现象 |
| (1)铝片与足量盐酸反应 | 铝片开始无现象,一段时间后逐渐溶解,并有大量气泡产生 |
| (2)铝片与足量硫酸反应 | 铝片开始无现象,一段时间后反应缓慢,有少量气泡产生 |
| (3)铝片与足量氢氧化钠溶液反应 | 铝片开始无现象,一段时间后逐渐溶解,并有大气泡产生 |
| A.刚开始无现象是因为铝片表面的 |
| B.对比实验(1)、(2)的酸的浓度,是为了消除 |
| C.对比实验(1)、(2)后来产生气泡的现象,可得出: |
| D.对比三个实验产生的现象和酸碱挥发性可推知:上述方案中实验(3)最适宜于实验室制备 |
为探究铍及其氧化物的性质,进行如下实验(铍片规格相同):
下列说法错误的是
| 实验操作 | 实验现象 | 实验原理 |
| ①向盛有铍片的试管中加入足量6mol•L-1盐酸 | 开始无现象,一段时间后铍片逐渐溶解,并有大量气泡产生 | BeO+2HCl=BeCl2+H2O Be+2HCl=BeCl2+H2↑ |
| ②向盛有铍片的试管中加入足量3mol•L-1硫酸溶液 | 开始无现象,一段时间后,铍片表面缓慢放出少量气泡 | BeO+H2SO4=BeSO4+H2O Be+H2SO4=BeSO4+H2↑ |
| ③向盛有铍片的试管中加入足量6mol•L-1氢氧化钠溶液 | 开始无现象,一段时间后铍片逐渐溶解,并有大量气泡产生 | BeO+2NaOH=Na2BeO2+H2O Be+2NaOH=Na2BeO2+H2↑ |
| A.实验开始均无现象原因是:Be在空气中形成氧化膜 |
| B.根据实验可知:BeO既有碱性氧化物的性质,又有酸性氧化物的性质 |
| C.对比实验①、②可知:c(H+)越大,相同时间内产生气泡越多 |
| D.对比实验①、②可知:Cl-对Be与H+的反应可能有促进作用 |
某实验小组将Cu片与30%双氧水混合,无反应现象,在此基础上分别又进行了三组对比实验,记录实验现象。
下列有关说法正确的是
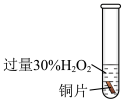 | 实验 | 现象 |
| ⅰ.加入 | 无明显现象 | |
| ⅱ.加入 | 开始产生少量气泡,溶液变为蓝色,片刻后,反应越来越剧烈,甚至形成大量泡沫涌出 | |
| ⅲ.加入1mL 0.2mol/L氨水 | 开始产生较多气泡,溶液变为深蓝色。一段时间后,反应逐渐变慢 |
| A.由反应ⅰ和ⅱ可知, |
| B.由反应ⅱ和ⅲ现象可知,两个反应的原理不同 |
| C.反应ⅲ产物为 |
| D.由反应ⅱ和ⅲ可推测,再加入 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


