解答题-实验探究题 适中0.65 引用1 组卷161
某小组利用 H2C2O4溶液与酸性 KMnO4溶液反应来探究“条件对化学反应 速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开 始计时。该小组设计了如下的方案。
(1)已知 H2C2O4被酸性 KMnO4氧化为 CO2逸出,该反应的化学方程式为_____ , 为了观察到实验现象从而判断反应的快慢,H2C2O4与 KMnO4初始的物质的量需要满足的关系为:n(H2C2O4):n(KMnO4)≥_____
(2)探究温度对化学反应速率影响的实验编号是_____ (填编号,下同),可探究H2C2O4浓度对化学反应速率影响的实验编号是_____
(3)实验①测得反应所用的时间为 40s,忽略混合前后溶液体积的微小变化,这段时间 内平均反应速率 v(KMnO4)=______ 。
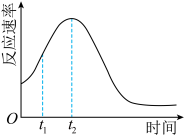
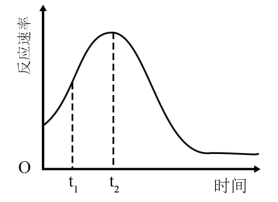
(4)该小组发现室温下反应速率走势如图,有同学认为其中 t1~t2时间内速率变快的主 要原因是反应放热导致反应体系温度升高,你认为还有可能是:_____ , 若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试 剂外,还需要选择的试剂最合理的是_____ (填序号)
A 硫酸钾 B 硫酸锰
C 稀硫酸 D 氯化锰
编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 蒸馏水体积/mL | 温度/℃ | ||
浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | |||
① | 0.50 | 6.0 | 0.010 | 4.0 | 0 | 25 |
② | 0.50 | 4.0 | 0.010 | 4.0 | 2.0 | 25 |
③ | 0.50 | 6.0 | 0.010 | 4.0 | 0 | 50 |
(2)探究温度对化学反应速率影响的实验编号是
(3)实验①测得反应所用的时间为 40s,忽略混合前后溶液体积的微小变化,这段时间 内平均反应速率 v(KMnO4)=
(4)该小组发现室温下反应速率走势如图,有同学认为其中 t1~t2时间内速率变快的主 要原因是反应放热导致反应体系温度升高,你认为还有可能是:
A 硫酸钾 B 硫酸锰
C 稀硫酸 D 氯化锰

20-21高二上·山西太原·阶段练习
类题推荐
同学们测定和探究影响反应速率的因素,设计了如下系列实验。
Ⅰ.甲同学测定室温下H2C2O4溶液与用硫酸酸化的KMnO4溶液的反应速率。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时。该小组设计了如下的方案。
(1)写出H2C2O4与KMnO4(H+)反应的离子反应方程式:___________
(2)该实验是通过测定___________ 来计算反应速率。
(3)实验测得反应所用的时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=___________ 。
(4)该小组发现室温下反应速率走势如图,其中t1~t2时间内速率变快的主要原因可能是:___________ ,若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是___________ (填序号)。
A.硫酸钾 B.硫酸锰 C.稀硫酸 D.二氯化锰
Ⅱ.乙同学利用控制变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
(5)该实验①、②可探究___________ 对反应速率的影响,因此V1和V3分别是___________ 、___________ 。实验①、③可探究硫酸浓度对反应速率的影响,因此V5=___________ 。
(6)硫代硫酸钠与稀硫酸反应离子反应方程式:___________ 。
Ⅰ.甲同学测定室温下H2C2O4溶液与用硫酸酸化的KMnO4溶液的反应速率。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时。该小组设计了如下的方案。
| H2C2O4溶液 | 酸性KMnO4溶液 | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL |
| 0.50 | 6.0 | 0.020 | 4.0 |
(2)该实验是通过测定
(3)实验测得反应所用的时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=
(4)该小组发现室温下反应速率走势如图,其中t1~t2时间内速率变快的主要原因可能是:
A.硫酸钾 B.硫酸锰 C.稀硫酸 D.二氯化锰

Ⅱ.乙同学利用控制变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
| 实验序号 | 反应温度/℃ | Na2S2O3浓度 | 稀硫酸 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| ③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
(6)硫代硫酸钠与稀硫酸反应离子反应方程式:
探究“外界条件对化学反应速率的影响”,可以用到定性分析、定量分析和对比分析等多种方法:
Ⅰ、H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
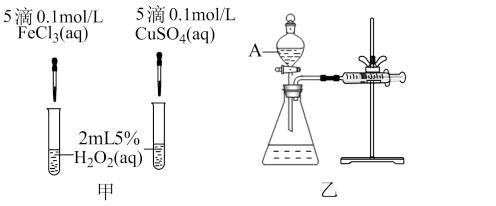
(1)若利用图甲装置,可通过观察_______ 现象,从而定性比较得出结论。
(2)有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_______ 。
(3)若利用乙实验可进行定量分析,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是_______ 。
Ⅱ、 某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案。
(4)已知反应后H2C2O4转化为CO2逸出,KMnO4溶液转化为MnSO4,每消耗1 mol H2C2O4转移_______ mol电子。为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4):n(KMnO4)≥_______ 。
(5)要探究温度对化学反应速率的影响,应选择的实验编号是_______ (填编号,下同),探究反应物浓度对化学反应速率的影响,应选择的实验编号是_______ 。
(6)该小组发现保持温度恒定,反应速率走势如图,其中t1~t2时间内速率变快的主要原因可能是:_______ ,若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是_______ (填序号)。

A.硫酸钾 B.硫酸锰 C.稀硫酸 D.二氯化锰
Ⅰ、H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。

(1)若利用图甲装置,可通过观察
(2)有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
(3)若利用乙实验可进行定量分析,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是
Ⅱ、 某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案。
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(5)要探究温度对化学反应速率的影响,应选择的实验编号是
(6)该小组发现保持温度恒定,反应速率走势如图,其中t1~t2时间内速率变快的主要原因可能是:

A.硫酸钾 B.硫酸锰 C.稀硫酸 D.二氯化锰
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡,混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案:
(1)已知反应后H2C2O4转化为CO2逸出,为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为:n(H2C2O4)∶n(KMnO4)______________ 。
(2)探究温度对化学反应速率影响的实验编号是_______ (填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是 ________ .
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=_______ 。
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度(mol/L) | 体积/mL | 浓度(mol/L) | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.01 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.01 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.01 | 4.0 | 50 |
(1)已知反应后H2C2O4转化为CO2逸出,为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为:n(H2C2O4)∶n(KMnO4)
(2)探究温度对化学反应速率影响的实验编号是
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


