单选题 适中0.65 引用1 组卷177
高铁酸钾(K2FeO4)作为多功能水处理剂具有广泛的用途,下面是利用次氯酸盐在碱性条件下氧化硝酸铁制备K2FeO4的生产工艺流程图:
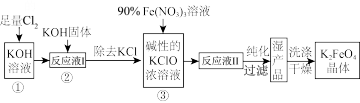
下列判断正确的是( )

下列判断正确的是( )
| A.反应①中氯气只起氧化剂的作用 |
| B.反应液I的溶质只有KClO |
| C.反应③中氧化剂与还原剂的物质的量之比为1:1 |
| D.反应液II的溶质成分中含有K2FeO4 |
20-21高三上·福建厦门·阶段练习
类题推荐
高铁酸钾(K2FeO4)是一种兼具净水和消毒功能的可溶性盐,可发生如下反应2K2FeO4+16HCl=4KCl+2FeCl3+8H2 O+3Q↑,下列说法不正确的是( )
| A.可用湿润的淀粉碘化钾试纸检验产物Q(Q能氧化I﹣) |
| B.K2FeO4在水中的电离方程式为K2FeO4 =2K++FeO42- |
| C.反应中氧化剂与还原剂的物质的量之比为1 :3 |
| D.反应中涉及的生成物可能有4种为电解质 |
新型净水剂高铁酸钾(K2FeO4)为暗紫色固体,可溶于水.工业上制备K2FeO4的常用方法之一是次氯酸盐氧化法:
①2FeCl3+10NaOH+3NaClO = 2Na2FeO4+9NaCl+5H2O ,
② Na2FeO4 + 2KOH = K2FeO4 + 2NaOH .
下列说法不正确 的是
①2FeCl3+10NaOH+3NaClO = 2Na2FeO4+9NaCl+5H2O ,
② Na2FeO4 + 2KOH = K2FeO4 + 2NaOH .
下列说法
| A.反应①为氧化还原反应,反应②为复分解反应 |
| B.反应①中NaClO 是氧化剂 |
| C.反应②的产物K2FeO4中Fe为+6价,具有强氧化性,能杀菌消毒 |
| D.反应①若有1 mol FeCl3 发生反应,转移电子的物质的量为 6 mol |
高铁酸钾(K2FeO4)是一种兼具净水和消毒功能的可溶性盐,可发生如下反应:2K2FeO4 + 16HCl → 4 KCl + 2FeCl3 + 8 H2 O + 3Q ↑,下列说法正确的是
| A.反应中涉及的6种物质均为电解质 |
| B.当电子转移0.5NA时,生成氯气5.6 L |
| C.可用湿润的淀粉碘化钾试纸检验产物Q |
| D.反应中氧化剂与还原剂的物质的量之比为1∶8 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


