解答题-原理综合题 适中0.65 引用3 组卷428
NH4Al(SO4)2和Na2CO3常作食品加工中的食品添加剂;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)纯碱Na2CO3溶液呈_________ (填“酸性”、“碱性”、“中性”),原因是________________________ (用离子方程式说明)。
(2)相同条件下,0.1 mol/L NH4Al(SO4)2溶液中的c( )
)________ (填“等于”“大于”或“小于”)0.1 mol/L NH4HSO4溶液中的c( )。
)。
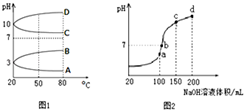
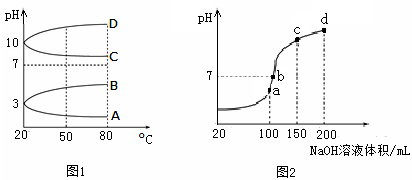
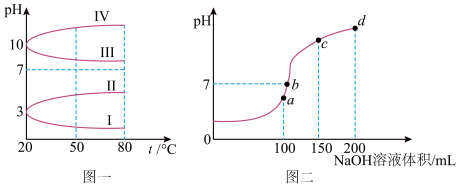
(3)均为0.1 mol/L的几种电解质溶液的pH随温度变化的曲线如图甲所示。
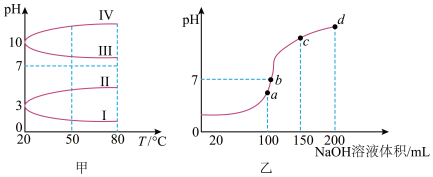
①其中符合0.1 mol/LNa2CO3溶液的pH随温度变化的曲线是________ (填罗马数字),导致Na2CO3溶液的pH随温度变化的原因是 _____________________________________ 。
②20℃时(Kw=1.0×10-14),0.1 mol/LNa2CO3溶液中c(Na+)-2c(CO32-)-c(HCO3-)=________ mol/L。
(4)室温时,向100 mL 0.1 mol/L NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图乙所示。试分析图中a、b、c、d四个点,水的电离程度最大的是__________ 点。在a点,溶液中各离子浓度由大到小的关系是 ___________________________ 。
(1)纯碱Na2CO3溶液呈
(2)相同条件下,0.1 mol/L NH4Al(SO4)2溶液中的c(
(3)均为0.1 mol/L的几种电解质溶液的pH随温度变化的曲线如图甲所示。

①其中符合0.1 mol/LNa2CO3溶液的pH随温度变化的曲线是
②20℃时(Kw=1.0×10-14),0.1 mol/LNa2CO3溶液中c(Na+)-2c(CO32-)-c(HCO3-)=
(4)室温时,向100 mL 0.1 mol/L NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图乙所示。试分析图中a、b、c、d四个点,水的电离程度最大的是
19-20高二上·海南海口·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网