解答题-实验探究题 较难0.4 引用1 组卷0
选择性催化还原是在有催化剂的条件下将NOx转变为N2和H2O,这是目前国外硝酸厂进行尾气治理普遍采用的一种方法.某小组同学拟验证NO.被氨气还原并测算其转化率.
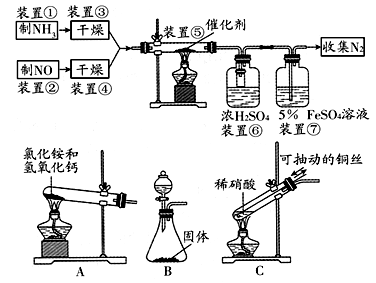
请回答下列问题:
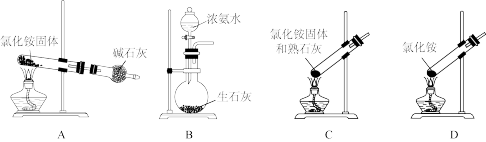
(1)若制取氨气用A装置,则发生反应的化学方程式为_____________________ ;若用B装置制取氨气,则分液漏斗和锥形瓶中盛放的药品分别是___________ ;
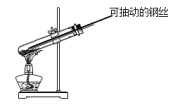
(2)用C装置制取NO时,用可抽动的铜丝,其优点是__________________________ ;其反应的离子方程式为____________________________________________ ;
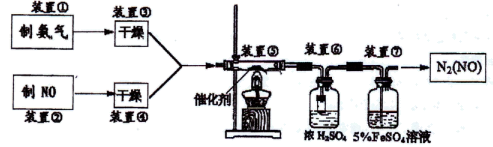
(3)装置⑦的作用可能是________________________________________ ;
(4)装置⑤中的化学方程式是_____________________________ ,若进入装置⑤的NO共2688 mL(标况下),氨气过量,最后收集到标况下2016 mL N2 ,则NO的转化率为___________ .

请回答下列问题:
(1)若制取氨气用A装置,则发生反应的化学方程式为
(2)用C装置制取NO时,用可抽动的铜丝,其优点是
(3)装置⑦的作用可能是
(4)装置⑤中的化学方程式是
18-19高一上·内蒙古赤峰·期末
类题推荐
有效的进行科学实验是学习化学的重要方法之一。
I.
(1)下列实验事实不能 作为所得结论合理证据的是_______ 。
II.选择性催化还原是在有催化剂的条件下将NOx转变为N2和H2O,这是目前硝酸厂进行尾气治理普遍采用的一种方法,某小组同学拟验证NO能被氨气还原并测算其转化率。
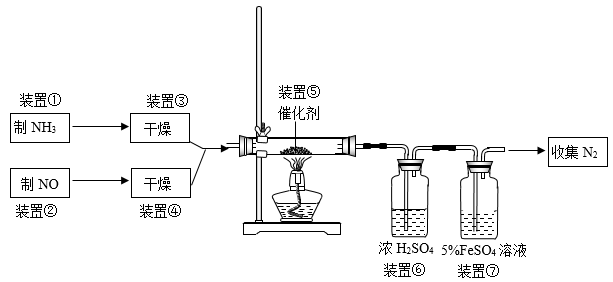
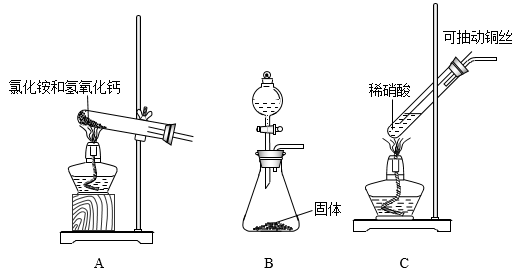
请回答下列问题:
(2)若制取氨气用A装置,则发生反应的化学方程式为_______ ,若用B装置制取氨气,则分液漏斗和锥形瓶中盛放的药品分别是_______ 、_______ ;
(3)用C装置制取NO时,用可抽动的铜丝,其优点是_______ ,其反应的离子方程式为_______ ;
(4)装置⑦的作用可能是_______ ;
(5)若进入装置⑤的NO共4.48L(标准状况下),氨气过量,最后收集到标况下2.24 LN2,则NO的转化率为_______ 。
III.常温常压下,一氧化二氯(Cl2O)为棕黄色气体,沸点为 3.8 ℃,42 ℃以上会分解生成 Cl2和 O2,Cl2O 易溶于水并与水反应生成 HClO。
【制备产品】将氯气和空气(不参与反应)按体积比 1:3 混合通入含水 8%的碳酸钠溶液中制备 Cl2O,并用水吸收 Cl2O(不含 Cl2)制备次氯酸溶液。
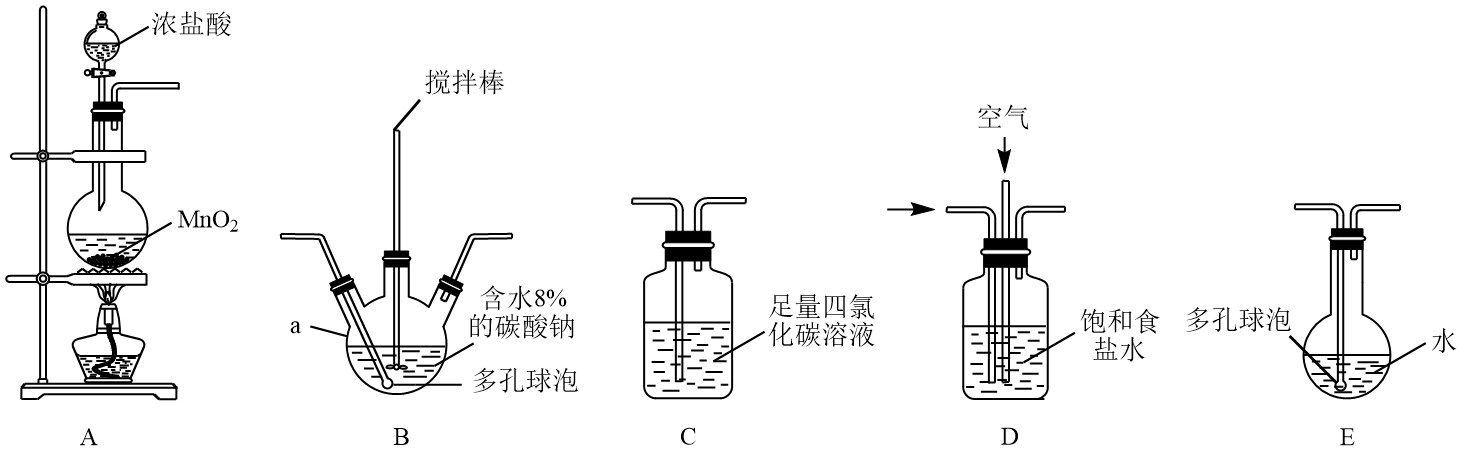
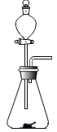
(6)各装置的连接顺序为_______ →_______ →_______ →C→_______ 。
(7)写出A中反应的离子方程式_______ 。
(8)制备Cl2O的化学方程式为_______ 。
(9)反应过程中,装置 B 需放在冷水中,其目的是_______ 。
(10)此方法相对于用氯气直接溶于水制备次氯酸溶液有两个主要优点,分别是_______ 、_______ 。
【测定浓度】
(11)用下列实验方案测定装置 E 所得溶液中次氯酸的物质的量浓度:量取10.00 mL上述次氯酸溶液,并稀释至100.00 mL,再从其中取出10.00 mL于锥形瓶中,并加入10.00 mL 0.8000 mol·L-1的FeSO4溶液(过量),充分反应后用0.05000 mol·L-1的酸性KMnO4溶液滴定剩余的 Fe2+,消耗 KMnO4溶液20.00 mL,则原次氯酸溶液的浓度为_______ 。判断下列情况对HClO含量测定结果的影响(填“偏高”、“偏低”或“无影响”)。若 FeSO4标准溶液部分变质,会使测定结果_______ ;若配制酸性KMnO4溶液时,定容时仰视视刻度线,会使测定结果_______ 。
I.
(1)下列实验事实
| 选项 | A | B | C | D |
| 实验 | 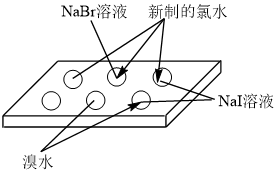 | 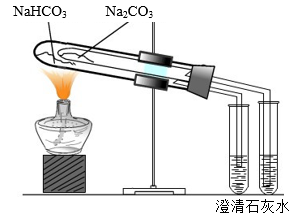 | 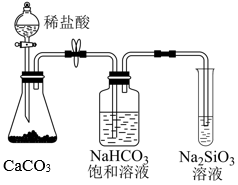 |  钾与水反应 钠与水反应 |
| 现象 | NaBr溶液变为橙色,NaI溶液变为棕黄色 | 左边盛澄清石灰水的试管变浑浊,而右边的不变浑浊 | Na2SiO3溶液中出现白色沉淀 | 钾与水反应比钠与水反应更剧烈 |
| 结论 | 氧化性:Cl2>Br2>I2 | 热稳定性:Na2CO3>NaHCO3 | 非金属性:C>Si | 金属性:K>Na |
II.选择性催化还原是在有催化剂的条件下将NOx转变为N2和H2O,这是目前硝酸厂进行尾气治理普遍采用的一种方法,某小组同学拟验证NO能被氨气还原并测算其转化率。


请回答下列问题:
(2)若制取氨气用A装置,则发生反应的化学方程式为
(3)用C装置制取NO时,用可抽动的铜丝,其优点是
(4)装置⑦的作用可能是
(5)若进入装置⑤的NO共4.48L(标准状况下),氨气过量,最后收集到标况下2.24 LN2,则NO的转化率为
III.常温常压下,一氧化二氯(Cl2O)为棕黄色气体,沸点为 3.8 ℃,42 ℃以上会分解生成 Cl2和 O2,Cl2O 易溶于水并与水反应生成 HClO。
【制备产品】将氯气和空气(不参与反应)按体积比 1:3 混合通入含水 8%的碳酸钠溶液中制备 Cl2O,并用水吸收 Cl2O(不含 Cl2)制备次氯酸溶液。

(6)各装置的连接顺序为
(7)写出A中反应的离子方程式
(8)制备Cl2O的化学方程式为
(9)反应过程中,装置 B 需放在冷水中,其目的是
(10)此方法相对于用氯气直接溶于水制备次氯酸溶液有两个主要优点,分别是
【测定浓度】
(11)用下列实验方案测定装置 E 所得溶液中次氯酸的物质的量浓度:量取10.00 mL上述次氯酸溶液,并稀释至100.00 mL,再从其中取出10.00 mL于锥形瓶中,并加入10.00 mL 0.8000 mol·L-1的FeSO4溶液(过量),充分反应后用0.05000 mol·L-1的酸性KMnO4溶液滴定剩余的 Fe2+,消耗 KMnO4溶液20.00 mL,则原次氯酸溶液的浓度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网