解答题-原理综合题 适中0.65 引用2 组卷143
甲醇作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
I. 甲醇可以替代汽油和柴油作为内燃机燃料。
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃、101 kPa时,1 mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出5518 kJ热量。该反应的热化学方程式为_________ 。
(2)某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如所示。
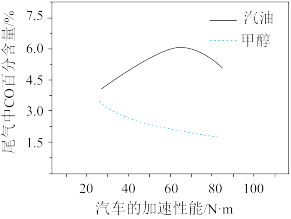
根据图信息分析,与汽油相比,甲醇作为燃料的优点是______ 。
II. 甲醇的合成
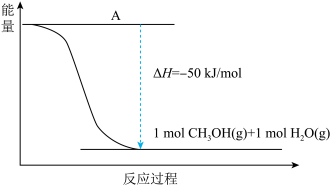
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。
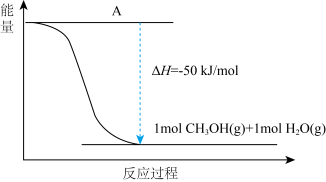
该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的ΔH______ (填“变大”“变小”或“不变”)。
(4)已知: CO(g)+ O2(g)= CO2(g) ΔH1=-283 kJ/mol
O2(g)= CO2(g) ΔH1=-283 kJ/mol
H2(g)+ O2(g) =H2O(g) ΔH2=-242 kJ/mol
O2(g) =H2O(g) ΔH2=-242 kJ/mol
CH3OH(g) + O2(g) =CO2(g) + 2H2O(g) ΔH3=-676 kJ/mol
O2(g) =CO2(g) + 2H2O(g) ΔH3=-676 kJ/mol
以CO(g)和H2(g)为原料合成甲醇的反应为CO(g) + 2H2(g)=CH3OH(g) 。该反应的ΔH为_____ kJ/mol。
(5)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:
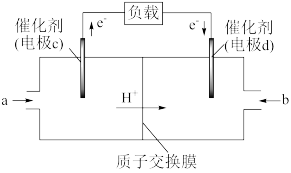
电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是_________ (填“正极”或“负极”),c电极的反应方程式为________ 。
I. 甲醇可以替代汽油和柴油作为内燃机燃料。
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃、101 kPa时,1 mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出5518 kJ热量。该反应的热化学方程式为
(2)某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如所示。

根据图信息分析,与汽油相比,甲醇作为燃料的优点是
II. 甲醇的合成
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。

该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的ΔH
(4)已知: CO(g)+
H2(g)+
CH3OH(g) +
以CO(g)和H2(g)为原料合成甲醇的反应为CO(g) + 2H2(g)=CH3OH(g) 。该反应的ΔH为
(5)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:

电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是
20-21高二上·四川成都·阶段练习
类题推荐
甲醇作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
Ⅰ.甲醇可以替代汽油和柴油作为内燃机燃料
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃,101KPa时,0.2mol辛烷完全燃烧生成气态二氧化碳和液态水,放出1103.6kJ热量。该反应的热化学方程式为___ 。25℃,101KPa时CH3OH(l)+ O2(g)=CO2(g)+2H2O(l)ΔH=-726.5kJ·mol-1,相同质量的甲醇和辛烷分别燃烧时释放的热量用于煅烧石灰石制备CaO,则得到CaO多的是
O2(g)=CO2(g)+2H2O(l)ΔH=-726.5kJ·mol-1,相同质量的甲醇和辛烷分别燃烧时释放的热量用于煅烧石灰石制备CaO,则得到CaO多的是___ (填“甲醇”或“辛烷”)。
(2)CH3OH(l)+O2(g)=CO(g)+2H2O(g)ΔH=-393kJ·mol-1,该反应相关化学键键能数据如下表:则X=___ 。
Ⅱ.甲醇的合成
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如图所示。___ 。
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应ΔH___ (填“变大”、“变小”或“不变”)。
③已知:CO(g)+ O2(g)=CO2(g) ΔH1=-283kJ·mol-1
O2(g)=CO2(g) ΔH1=-283kJ·mol-1
H2(g)+ O2(g)=H2O(g) ΔH2=-242kJ·mol-1
O2(g)=H2O(g) ΔH2=-242kJ·mol-1
CH3OH(g)+ O2(g)=CO2(g)+2H2O(g) ΔH3=-676kJ·mol-1
O2(g)=CO2(g)+2H2O(g) ΔH3=-676kJ·mol-1
以CO(g)和H2(g)为原料合成甲醇的热化学方程式为___ 。
Ⅰ.甲醇可以替代汽油和柴油作为内燃机燃料
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃,101KPa时,0.2mol辛烷完全燃烧生成气态二氧化碳和液态水,放出1103.6kJ热量。该反应的热化学方程式为
(2)CH3OH(l)+O2(g)=CO(g)+2H2O(g)ΔH=-393kJ·mol-1,该反应相关化学键键能数据如下表:则X=
| 化学键 | O=O | C-O | C≡O | H-O | C-H |
| E/(kJ·mol-1) | 496 | 343 | 1076 | X | 413 |
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如图所示。

②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应ΔH
③已知:CO(g)+
H2(g)+
CH3OH(g)+
以CO(g)和H2(g)为原料合成甲醇的热化学方程式为
甲醇作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
Ⅰ甲醇可以替代汽油和柴油作为内燃机燃料
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃,101KPa 时,1mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出 5518kJ 热量。该反应的热化学方程式为:_____
(2)已知:25℃,101KPa 时,CH3OH(l)+ 3/2 O2(g)=CO2(g)+2H2O(l) ΔH=-726.5 kJ·mol-1
相同质量的甲醇和辛烷分别燃烧时,放出热量最多的是_____ (填化学式)
(3)CH3OH(l)+ O2(g)=CO(g)+2H2O(g) ΔH=-393 kJ·mol-1该反应相关化学键键能数据如下表:
则 X=_____ 。
Ⅱ甲醇的合成
(4)以 CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如图所示。
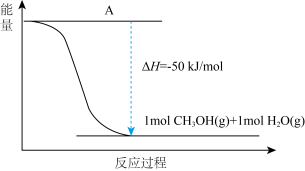
①补全上图:图中A 处应填入_____ 。
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应 ΔH_____ (填“变大”“变小”“不变”)。
③已知:
CO(g)+ 1/2 O2(g) = CO2(g) ΔH1=-283kJ·mol-1
H2(g)+ 1/2 O2(g) = H2O(g)ΔH2=-242kJ·mol-1
CH3OH(g)+ 3/2 O2(g)=CO2(g)+2H2O(g) ΔH3=-676 kJ·mol-1
以 CO(g)和 H2(g)为原料合成甲醇的反应为 CO(g)+ 2H2(g) = CH3OH(g),该反应的 ΔH=_____ kJ·mol-1。
Ⅰ甲醇可以替代汽油和柴油作为内燃机燃料
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃,101KPa 时,1mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出 5518kJ 热量。该反应的热化学方程式为:
(2)已知:25℃,101KPa 时,CH3OH(l)+ 3/2 O2(g)=CO2(g)+2H2O(l) ΔH=-726.5 kJ·mol-1
相同质量的甲醇和辛烷分别燃烧时,放出热量最多的是
(3)CH3OH(l)+ O2(g)=CO(g)+2H2O(g) ΔH=-393 kJ·mol-1该反应相关化学键键能数据如下表:
| 化学键 | O=O | C-O | C=O | H-O | C-H |
| E/( kJ·mol-1) | X | 343 | 1076 | 465 | 413 |
Ⅱ甲醇的合成
(4)以 CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如图所示。

①补全上图:图中A 处应填入
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应 ΔH
③已知:
CO(g)+ 1/2 O2(g) = CO2(g) ΔH1=-283kJ·mol-1
H2(g)+ 1/2 O2(g) = H2O(g)ΔH2=-242kJ·mol-1
CH3OH(g)+ 3/2 O2(g)=CO2(g)+2H2O(g) ΔH3=-676 kJ·mol-1
以 CO(g)和 H2(g)为原料合成甲醇的反应为 CO(g)+ 2H2(g) = CH3OH(g),该反应的 ΔH=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网