多选题 适中0.65 引用2 组卷88
将CH4设计成燃料电池,其利用率更高,装置示意如图(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积VL。则下列说法错误的是( )
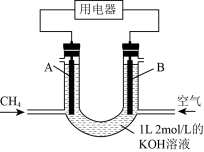

| A.通入CH4的一端为原电池的负极,通入空气的一端为原电池的正极 |
| B.0<V≤22.4L电池总反应的化学方程式为CH4+2O2+2KOH=K2CO3+3H2O |
| C.22.4 L<V≤44.8 L时,负极电极反应为CH4-8e-+2H2O=CO2+8H+ |
| D.V=33.6 L时,溶液中只存在阴离子 |
20-21高二上·河北沧州·阶段练习
类题推荐
将甲烷设计成燃料电池,其利用率更高,如图所示(A, B为多孔性碳棒)。持续通入甲烷,在标准状况下,消耗甲烷体积VL,则下列说法错误的是
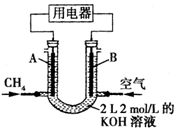

| A.通入CH4的一端为原电池的负极,溶液中OH-向负极区移动 |
| B.当0<V ≤22.4L时,电池总反应式为CH4+2O2+2KOH=K2CO3+3H2O |
| C.当22.4L<V≤44.8L时,负极电极反应为CH4-8e-+9CO32-+3H2O=10HCO3- |
| D.当V=33.6L时,溶液中阴离子浓度大小关系为c(CO32-)>c(HCO3-)>c(OH-) |
天然气的主要成分为CH4,可将CH4设计成燃料电池,来解决能源问题,装置如图所示。在标准状况下,持续通入甲烷,消耗甲烷VL。下列说法错误 的是

| A.当0<V≤33.6 L时,负极反应式为 CH4+10OH--8e-== CO32-+7H2O |
| B.正极反应式为O2 +4H+ +4e-==2H2O |
| C.当V=67.2 L时,电池总反应方程式可写为 CH4+2O2+NaOH== NaHCO3+2H2O |
| D.电解质溶液中的Na+向正极移动 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网