单选题 适中0.65 引用6 组卷411
某小组利用电导率(电导率越大,导电能力越强)传感器、pH传感器探究NaHCO3和CaCl2能否发生化学反应。向25.00mL0.1mol•L-1NaHCO3溶液中滴入等体积、等浓度CaCl2溶液,电导率以及pH变化曲线如图所示。下列说法错误的是
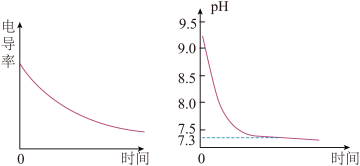

| A.电导率下降的原因是生成了CaCO3沉淀导致溶液中离子浓度降低 |
| B.pH下降的原因是Ca2+促进 |
| C.pH=7.3时溶液中溶质主要为NaCl、CaCl2 |
| D.可用0.1mol•L-1CaCl2溶液鉴别浓度均为0.1mol•L-l的NaHCO3和Na2CO3溶液 |
2020·湖北武汉·模拟预测
类题推荐
用0.100mol·L-1的NaOH溶液分别滴定体积均为10.00mL、浓度均为0.100mol·L-1的HCl和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率(电导率越大表示溶液导电性越强)变化如图所示。下列说法正确的是


| A.曲线①代表向HCl中滴加NaOH | B.A点溶液的pH小于C点溶液的pH |
| C.A、B两点水的电离程度:A>B | D.C→D发生了反应:H++OH-=H2O |
已知电导率可用于衡量电解质溶液导电能力大小,且电导率越大溶液的导电能力越强。某兴趣小组利用pH和电导率传感器对铜氨配合物的形成过程进行探究,向60mL 0.02mol/L CuSO4溶液中滴加0.04 mol/L氨水,先产生Cu(OH)2沉淀,后沉淀溶解生成Cu(NH3) ,得到的pH曲线和电导率曲线如图所示。下列说法错误的是
,得到的pH曲线和电导率曲线如图所示。下列说法错误的是
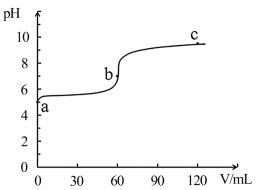



| A.a点显酸性的原因是Cu2++2H2O |
| B.d→e电导率增大的原因是溶液中离子浓度逐渐增加 |
| C.b点:c(NH |
| D.b→c离子方程式为:Cu(OH)2 + 4NH3 ▪H2O = Cu(NH3) |
电解质的电导率越大,导电能力越强。用0.100mol•L-1的KOH溶液分别滴定体积均为20.00mL、浓度均为0.100mol·L-1的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
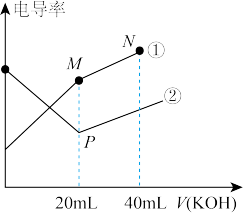

| A.曲线②代表滴定CH3COOH溶液的曲线 |
| B.在相同温度下,水的电离程度:P>M>N |
| C.M点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.1mol•L-1 |
| D.N点溶液中:c(K+)>c(OH-)>c(CH3COO-)>c(H+) |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


