解答题-无机推断题 较难0.4 引用2 组卷401
A、B、C、D是原子序数依次递增的四种短周期元素。基态A原子所含的电子只有一种运动状态;基态B原子中有三个未成对电子。A、B、C、D四种元素共同组成化合物M,M可发生如下反应:
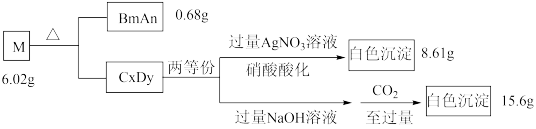
回答下列问题:
(1)B原子的价电子排布式为_______ 。实验室制备BmAn的化学方程式是_________ 。
(2)A、C、D三种元素的原子半径由大到小的顺序为_________ (用元素符号表示)。
(3)B元素的第一电离能比同周期相邻两种元素的都高;原因是____________ 。
(4) D元素的一种氧化物D2O为淡棕黄色气体,可由新制的HgO和D2发生歧化反应(氧化剂和还原剂为同一种物质的反应)制得。上述制备D2O的化学方程式为_________ 。
(5)D元素的另一种氧化物DO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaDO2、NaHSO4、NaHCO3的泡腾片,能快速溶于水,溢出大量气泡,得到DO2溶液。上述过程中,生成DO2的反应属于歧化反应,每生成1 mol DO2消耗NaDO2的量为_____ mol;若产生的“气泡”与DO2的物质的量相等,则反应过程中消耗NaDO2、NaHSO4、NaHCO3的物质的量之比为____________ 。
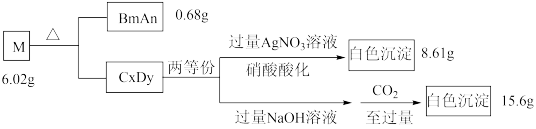
回答下列问题:
(1)B原子的价电子排布式为
(2)A、C、D三种元素的原子半径由大到小的顺序为
(3)B元素的第一电离能比同周期相邻两种元素的都高;原因是
(4) D元素的一种氧化物D2O为淡棕黄色气体,可由新制的HgO和D2发生歧化反应(氧化剂和还原剂为同一种物质的反应)制得。上述制备D2O的化学方程式为
(5)D元素的另一种氧化物DO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaDO2、NaHSO4、NaHCO3的泡腾片,能快速溶于水,溢出大量气泡,得到DO2溶液。上述过程中,生成DO2的反应属于歧化反应,每生成1 mol DO2消耗NaDO2的量为
19-20高三·山东潍坊·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


