解答题-原理综合题 适中0.65 引用1 组卷465
在化学科学研究中,物质发生化学反应的反应热可通过实验测定,也可通过化学计算的方式间接获得。
(1)实验方法测定反应热
①中和反应反应热的测定
实验中所需要使用的仪器除量热计外,还需要的玻璃仪器有__ 。为了减少实验误差,实验过程中应将NaOH溶液__ (填“一次性”或“分多次”)倒入盛有盐酸的量热计内筒中;溶液混合后,准确读取混合溶液的___ ,记为终止温度。
②实验测得在一定温度下,0.2molCH4(g)与足量H2O(g)完全反应生成CO2(g)和H2(g)吸收33kJ的热量,该反应的热化学方程式为__ 。
(2)通过化学计算间接获得反应热
①已知断裂1molH—H键、I—I键、H—I键需要吸收的能量分别为436kJ、153kJ、299kJ。则反应H2(g)+I2(g)=2HI(g)的△H=___ kJ•mol-1。
②已知:CO(g)+2H2(g)=CH3OH(g) △H1=-90.8kJ•mol-1;
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ•mol-1;
H2(g)+ O2(g)=H2O(g) △H3=-241.8kJ•mol-1。
O2(g)=H2O(g) △H3=-241.8kJ•mol-1。
根据上述反应计算H2的燃烧热△H=__ kJ•mol-1;
CH3OH(g)+O2(g)=CO(g)+2H2O(g)△H=__ kJ•mol-1。
(1)实验方法测定反应热
①中和反应反应热的测定
实验中所需要使用的仪器除量热计外,还需要的玻璃仪器有
②实验测得在一定温度下,0.2molCH4(g)与足量H2O(g)完全反应生成CO2(g)和H2(g)吸收33kJ的热量,该反应的热化学方程式为
(2)通过化学计算间接获得反应热
①已知断裂1molH—H键、I—I键、H—I键需要吸收的能量分别为436kJ、153kJ、299kJ。则反应H2(g)+I2(g)=2HI(g)的△H=
②已知:CO(g)+2H2(g)=CH3OH(g) △H1=-90.8kJ•mol-1;
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ•mol-1;
H2(g)+
根据上述反应计算H2的燃烧热△H=
CH3OH(g)+O2(g)=CO(g)+2H2O(g)△H=
19-20高二·全国·课时练习
类题推荐
(一)实验方法测定反应热---------中和热测定
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol· L-1盐酸、0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是 、 。
(2)他们记录的实验数据如下:
已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18KJ·℃-1· kg-1,各物质的密度均为1g·cm-3。
计算完成上表。△H=
(3)某研究小组将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50 mL)。回答下列问题:
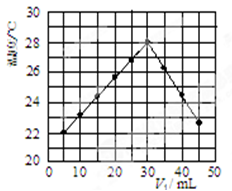
研究小组做该实验时环境温度 (填“高于”、“低于”或“等于”)22 ℃,此反应所用NaOH溶液的浓度应为 mol/L。
(二)通过化学计算间接获得
(1)已知拆开1mol的H—H键、I—I、H—I键分别需要吸收的能量为436kJ、153kJ、299kJ。
则反应H2(g)+I2(g)=2HI(g)的反应热△H= kJ·mol-1
(2)已知:2H2(g)+ O2(g) = 2H2O (l) △H=-571.6 kJ·mol-1
H2(g)+1/2O2(g) = H2O(g) △H=-241.8 kJ·mol-1
根据上述反应确定:H2燃烧热为 kJ·mol-1;
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol· L-1盐酸、0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是 、 。
(2)他们记录的实验数据如下:
| 实 验 用 品 | 溶 液 温 度 | 中和热△H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18KJ·℃-1· kg-1,各物质的密度均为1g·cm-3。
计算完成上表。△H=
(3)某研究小组将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50 mL)。回答下列问题:

研究小组做该实验时环境温度 (填“高于”、“低于”或“等于”)22 ℃,此反应所用NaOH溶液的浓度应为 mol/L。
(二)通过化学计算间接获得
(1)已知拆开1mol的H—H键、I—I、H—I键分别需要吸收的能量为436kJ、153kJ、299kJ。
则反应H2(g)+I2(g)=2HI(g)的反应热△H= kJ·mol-1
(2)已知:2H2(g)+ O2(g) = 2H2O (l) △H=-571.6 kJ·mol-1
H2(g)+1/2O2(g) = H2O(g) △H=-241.8 kJ·mol-1
根据上述反应确定:H2燃烧热为 kJ·mol-1;
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 2NH3(g)ΔH=akJ•mol-1,根据下表中所列键能数据可计算出a=
2NH3(g)ΔH=akJ•mol-1,根据下表中所列键能数据可计算出a=

