解答题-无机推断题 适中0.65 引用1 组卷125
部分中学化学常见元素原子结构及性质如下表所示。
(1)这五种元素的原子半径由大到小的顺序为_______________ (用元素符号表示)。
(2)E与D可以按原子个数比2:1、1:1形成两种化合物X、Y,区别X、Y这两种物质的实验方案为________ 。E与C组成的两种化合物M、N,所含电子数分别与X、Y相等,M中共用电子对对数为_______________ ,N的结构式为_______________ 。
(3)A与C可以形成一种新型陶瓷材料,机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是_______________ 。
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发此种陶瓷的全陶发动机替代同类型金属发动机
D.此种陶瓷的开发受到资源的限制,没有发展前途
| 序号 | 元素 | 结构及性质 |
| ① | A | A为地壳中含量仅次于氧的非金属元素,其单质晶体结构与金刚石相似 |
| ② | B | B原子最外层电子数是内层电子总数的1/5 |
| ③ | C | C是常用化肥的主要元素,单质常温下呈气态 |
| ④ | D | 通常情况下,D在化合物中显负价,A、B、C都能与D形成中学常见化合物 |
| ⑤ | E | E是宇宙中最丰富的元素 |
(1)这五种元素的原子半径由大到小的顺序为
(2)E与D可以按原子个数比2:1、1:1形成两种化合物X、Y,区别X、Y这两种物质的实验方案为
(3)A与C可以形成一种新型陶瓷材料,机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发此种陶瓷的全陶发动机替代同类型金属发动机
D.此种陶瓷的开发受到资源的限制,没有发展前途
20-21高三上·湖北黄冈·阶段练习
类题推荐
(1)部分中学化学常见元素的原子结构及性质如下表所示。
①这五种元素的原子半径最大是______ (用元素符号表示)。
②E与D可以按原子个数比2:1、1:1形成两种化合物X、Y, E与C组成的两种化合物M、N,所含电子数分别与X、Y相等,M中共用电子对对数为______ ,N的结构式为______ 。
(2)已知:某无色废水中可能含有H+、NH 、Fe3+、Al3+、Mg2+、Na+、NO
、Fe3+、Al3+、Mg2+、Na+、NO 、CO
、CO 、SO
、SO 中的几种,为分析其成分,分别取废水样品1 L,进行了三组实验,其操作和有关图象如下所示:
中的几种,为分析其成分,分别取废水样品1 L,进行了三组实验,其操作和有关图象如下所示:
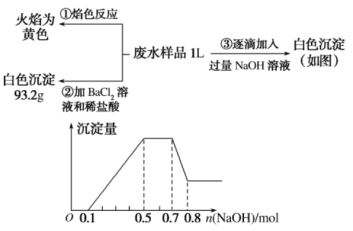
请回答下列问题:
①根据上述3组实验可以分析废水中一定不存在的阴离子是______ 。
②写出实验③图象中沉淀达到最大量且质量不再发生变化阶段发生反应的离子方程式______ 。
③分析图象,所得沉淀的最大质量是______ g。
④若通过实验确定原废水中c(Na+)=0.18 mol·L-1,试判断原废水中NO 是否存在
是否存在______ ,若存在,c(NO )=
)=______ mol·L-1 (若不存在或不确定则此空不填)。
| 元素 | 结构及性质 |
| A | A为地壳中含量仅次于氧的非金属元素,其单质晶体结构与金刚石相似 |
| B | B原子最外层电子数是内层电子总数的1/5 |
| C | C是常用化肥的主要元素,单质常温下呈气态 |
| D | 通常情况下,D在化合物中显负价,A、B、C都能与D形成中学常见化合物 |
| E | E元素的一种同位素原子无中子 |
②E与D可以按原子个数比2:1、1:1形成两种化合物X、Y, E与C组成的两种化合物M、N,所含电子数分别与X、Y相等,M中共用电子对对数为
(2)已知:某无色废水中可能含有H+、NH

请回答下列问题:
①根据上述3组实验可以分析废水中一定不存在的阴离子是
②写出实验③图象中沉淀达到最大量且质量不再发生变化阶段发生反应的离子方程式
③分析图象,所得沉淀的最大质量是
④若通过实验确定原废水中c(Na+)=0.18 mol·L-1,试判断原废水中NO
部分中学化学常见元素原子结构及性质如表所示:
(1)A元素在周期表中的位置为_____________________________________ 。
(2)B原子核外电子云有_____ 种伸展方向,B与C形成的化合物的化学式为________ 。
(3)①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,区别X与Y的水溶液的实验方法是_____________ 。
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的水溶液显______ 性,N的结构式为________ 。
③C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱______ 。
(4)有人认为B、D的单质用导线连接后插入NaOH溶液中可以形成原电池,你认为是否可以,若可以,试写出负极的电极方程式(若认为不行可不写)__________________ 。
| 序号 | 元素 | 结构及性质 |
| ① | A | A单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5 |
| ② | B | B原子最外层电子数是内层电子总数的1/5 |
| ③ | C | C是常见化肥的主要元素,单质常温下呈气态 |
| ④ | D | D原子核外电子运动状态有13种 |
| ⑤ | E | 通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物 |
| ⑥ | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
(2)B原子核外电子云有
(3)①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,区别X与Y的水溶液的实验方法是
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的水溶液显
③C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱
(4)有人认为B、D的单质用导线连接后插入NaOH溶液中可以形成原电池,你认为是否可以,若可以,试写出负极的电极方程式(若认为不行可不写)
部分中学化学常见元素原子结构及性质如表所示:
(1)A元素在周期表中的位置为____________________________________________ 。
(2)B与C形成的化合物的化学式为________ ,它属于________ (填“离子”或“共价”)化合物。
(3)①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,区别X与Y的水溶液的实验方法是____________________
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的水溶液显________ 性,N的结构式为________ 。
(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱____ 。
(5)有人认为B、D的单质用导线连接后插入氯化钠溶液中可以形成原电池,你认为是否可以,若可以,试写出正极的电极方程式(若认为不行可不写)___________________
| 序号 | 元素 | 结构及性质 |
| A | A单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5 | |
| B | B原子最外层电子数是内层电子总数的1/5 | |
| ③ | C | C是常见化肥的主要元素,单质常温下呈气态 |
| ④ | D | D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
| ① | E | 通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物 |
| ② | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
(1)A元素在周期表中的位置为
(2)B与C形成的化合物的化学式为
(3)①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,区别X与Y的水溶液的实验方法是
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的水溶液显
(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱
(5)有人认为B、D的单质用导线连接后插入氯化钠溶液中可以形成原电池,你认为是否可以,若可以,试写出正极的电极方程式(若认为不行可不写)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


