解答题-原理综合题 适中0.65 引用1 组卷260
(1)常温下,某溶液中由水电离出的离子浓度符合 的溶液,其pH为
的溶液,其pH为________ ,此时水的电离受到________ (填“促进”或“抑制”)。
(2)已知:
 。一定温度下,在密闭容器中反应
。一定温度下,在密闭容器中反应 达到平衡。其他条件不变时,下列措施能提高NO2转化率的是
达到平衡。其他条件不变时,下列措施能提高NO2转化率的是____ (填序号)。
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(3)在某温度下,H2O的离子积常数为1×10-13,则该温度下:
① 溶液的pH=
溶液的pH=________ 。
② 溶液与
溶液与 的
的 溶液混合后,pH=
溶液混合后,pH= ________ 。
(4)已知一溶液有4种离子: 、
、 、
、 、
、 ,下列分析结果肯定错误的是
,下列分析结果肯定错误的是________ (填序号)。
A. B.
B.
C. D.
D.
(5)在25℃下,将 的氨水与
的氨水与 的盐酸等体积混合,反应时溶液中
的盐酸等体积混合,反应时溶液中 ,则溶液显
,则溶液显_____ (填“酸”“碱”或“中”)性;用含a的代数式表示 的电离常数Kb=
的电离常数Kb=______ 。
(6)水溶液中的行为是中学化学的重要内容。已知下列物质的电离常数值(25℃):


 ,
, 
“84消毒液”中通入少量的CO2,该反应的化学方程式为________ 。
(2)已知:
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(3)在某温度下,H2O的离子积常数为1×10-13,则该温度下:
①
②
(4)已知一溶液有4种离子:
A.
C.
(5)在25℃下,将
(6)水溶液中的行为是中学化学的重要内容。已知下列物质的电离常数值(25℃):
“84消毒液”中通入少量的CO2,该反应的化学方程式为
19-20高二·全国·课时练习
类题推荐
(1)常温下某溶液中由水电离出的离子浓度符合c(H+)·c(OH﹣)=1×10﹣20的溶液,其pH为 ,此时水的电离受到 .
(2)在某温度下,H2O的离子积常数为1×10﹣13 mol2·L﹣2,则该温度下:100mL 0.1mol·L﹣1H2SO4溶液与100mL 0.4mol·L﹣1的KOH溶液混合后,pH= .
(3)已知一溶液有4种离子:X+、Y﹣、H+、OH﹣,下列分析结果肯定错误的是 .
(4)在25℃下,将a mol·L﹣1的氨水与0.01mol·L﹣1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl﹣).则溶液显 (填“酸”“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb= .
(5)水溶液中的行为是中学化学的重要内容.已知下列物质的电离常数值:HClO:Ka=3×10﹣8;H2CO3:Ka1=4.3×10﹣7;Ka2=5.6×10﹣11;84消毒液中通入少量的CO2,该反应的化学方程式为 .
(2)在某温度下,H2O的离子积常数为1×10﹣13 mol2·L﹣2,则该温度下:100mL 0.1mol·L﹣1H2SO4溶液与100mL 0.4mol·L﹣1的KOH溶液混合后,pH= .
(3)已知一溶液有4种离子:X+、Y﹣、H+、OH﹣,下列分析结果肯定错误的是 .
| A.c(Y﹣)>c(X+)>c(H+)>c(OH﹣) |
| B.c(X+)>c(Y﹣)>c(OH﹣)>c(H+) |
| C.c(H+)>c(Y﹣)>c(X+)>c(OH﹣) |
| D.c(OH﹣)>c(X+)>c(H+)>c(Y﹣) |
(4)在25℃下,将a mol·L﹣1的氨水与0.01mol·L﹣1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl﹣).则溶液显 (填“酸”“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb= .
(5)水溶液中的行为是中学化学的重要内容.已知下列物质的电离常数值:HClO:Ka=3×10﹣8;H2CO3:Ka1=4.3×10﹣7;Ka2=5.6×10﹣11;84消毒液中通入少量的CO2,该反应的化学方程式为 .
水溶液中的行为是中学化学的重要内容.已知水在25℃和95℃时的电离平衡曲线如图所示:
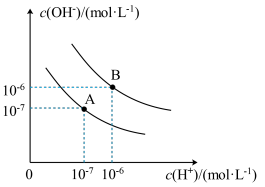
(1)25℃时水的电离平衡曲线应为_______ (填“A”或“B”)。
(2)25℃ 时,某溶液中由水电离出c(H+)=1×10﹣10 mol/L,该溶液pH为________ .
(3)在曲线B对应的温度下,将pH=2的某HA溶液和pH=10的NaOH溶液等体积混合,所得溶液的pH=5。请分析其原因:___________ 。
(4)电离常数是衡量弱电解质电离程度强弱的物理量.已知:
25℃时,将浓度相同的四种盐溶液:①NaCN②NaClO③Na2CO3④NaHCO3,按pH由大到小的顺序_____ (填序号),向84消毒液中通入少量的CO2,该反应的化学方程式为_______ 。
(5)25℃ 时,将n mol•L﹣1的氨水与0.2mol•L﹣1的盐酸等体积混合,反应平衡时溶液中c( )=c(Cl﹣),则溶液显
)=c(Cl﹣),则溶液显________ 性(填“酸”、“碱”或“中”),NH3•H2O的电离常数Kb=________ (用含n的代数式表示).

(1)25℃时水的电离平衡曲线应为
(2)25℃ 时,某溶液中由水电离出c(H+)=1×10﹣10 mol/L,该溶液pH为
(3)在曲线B对应的温度下,将pH=2的某HA溶液和pH=10的NaOH溶液等体积混合,所得溶液的pH=5。请分析其原因:
(4)电离常数是衡量弱电解质电离程度强弱的物理量.已知:
化学式 | HCN | HClO | H2CO3 |
电离常数(25℃ ) | K=4.9×10-10 | K=3×10-8 | K1=4.3×10-7、K2=5.6×10-11 |
25℃时,将浓度相同的四种盐溶液:①NaCN②NaClO③Na2CO3④NaHCO3,按pH由大到小的顺序
(5)25℃ 时,将n mol•L﹣1的氨水与0.2mol•L﹣1的盐酸等体积混合,反应平衡时溶液中c(
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


