填空题 适中0.65 引用4 组卷525
某化学兴趣小组为了研究部分ⅥA族元素及其化合物的部分性质,查阅资料如下:
①酸性: ;
;
②O、S、 与
与 的化合越来越难,
的化合越来越难, 与
与 不能直接化合;
不能直接化合;
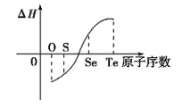
③由不同元素的单质生成等物质的量的氢化物的焓变情况如图所示。
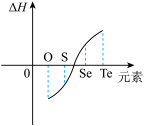
请回答下列问题:
(1)S与 的化合反应
的化合反应_________ (填“吸收”或“放出”)热量。
(2)已知 的分解反应的
的分解反应的 ,请解释
,请解释 与
与 不能直接化合的原因
不能直接化合的原因______________ 。
(3)题述信息中能说明S的非金属性强于 的是
的是_________ (填序号)。
①酸性:
②O、S、
③由不同元素的单质生成等物质的量的氢化物的焓变情况如图所示。

请回答下列问题:
(1)S与
(2)已知
(3)题述信息中能说明S的非金属性强于
18-19高二·全国·课时练习
类题推荐
某化学兴趣小组,专门研究了氧族元素及其某些化合物的部分性质。查得的资料如下:
①常温下,硒(Se)和碲(Te)为固体,H2Se和H2Te为气体;
②Te和H2不能直接化合生成H2Te;
③氧气、硫、硒、碲与1 mol H2反应的焓变(△H)情况如下表所示。
请回答下列问题:
(1)写出氧族元素中含有18个电子的两种氢化物的化学式_________ 、__________ 。
(2)写出硒化氢发生分解反应的热化学方程式:________________________________ 。
(3)已知H2Te分解反应的ΔS>0,ΔH=-154 kJ·mol-1,请解释Te和H2不能直接化合的原因______________________________________________________________________________________________________________________________________________ 。
(4)H2S的水溶液显弱酸性,写出其电离方程式_______________________________ ;它的第一级电离常数可用Ka1来表示,当温度升高时,Ka1的值________________ (填“一定增大”、“一定减小”或“不能确定”)。
(5)在容积均为1 L(容器体积不可变)的甲、乙两个容器中,分别充入2 mol SO2、1 molO2和4 mol SO2、2 mol O2,在相同条件下使其反应。最终达到平衡后,甲、乙两容器中SO2转化率分别为50%和α(乙),则反应的平衡常数Kc=____________ L·mol-1(填写具体数据),此时α(乙)______ 50%(填“大于”、“小于”或“等于”)。
①常温下,硒(Se)和碲(Te)为固体,H2Se和H2Te为气体;
②Te和H2不能直接化合生成H2Te;
③氧气、硫、硒、碲与1 mol H2反应的焓变(△H)情况如下表所示。
| 物质 | O2 | S | Se | Te |
| ΔH(kJ·mol-1) | -242 | -20 | 81 |
(1)写出氧族元素中含有18个电子的两种氢化物的化学式
(2)写出硒化氢发生分解反应的热化学方程式:
(3)已知H2Te分解反应的ΔS>0,ΔH=-154 kJ·mol-1,请解释Te和H2不能直接化合的原因
(4)H2S的水溶液显弱酸性,写出其电离方程式
(5)在容积均为1 L(容器体积不可变)的甲、乙两个容器中,分别充入2 mol SO2、1 molO2和4 mol SO2、2 mol O2,在相同条件下使其反应。最终达到平衡后,甲、乙两容器中SO2转化率分别为50%和α(乙),则反应的平衡常数Kc=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网