单选题 适中0.65 引用1 组卷105
锌-空气电池(原理 如图)适宜用作城市电动车的动力电源。该电池放电时Zn转化为ZnO。下列说法正确的是()
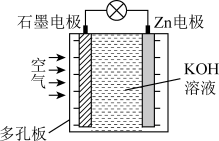

| A.每消耗1 mol O2转移2 mol电子 |
| B.氧气在石墨电极上发生氧化反应 |
| C.该电池放电时OH-向Zn电极移动 |
| D.该电池的负极反应为Zn+H2O-2e-=ZnO+2H+ |
19-20高一下·江苏泰州·阶段练习
类题推荐
锌—空气电池(原理如图)适宜用作城市电动车的动力电源。该电池放电时Zn转化为ZnO。该电池工作时,下列说法正确的是
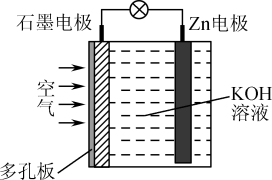

| A.K+向锌电极移动 |
| B.石墨电极是该电池的负极 |
| C.Zn电极的电极反应式:Zn+2OH--2e-=ZnO+H2O |
| D.当电路中流过2mol电子,消耗O2的体积为22.4L(标准状况下) |
锌一空气电池(原理如图所示)适宜用作城市电动车的动力电源。该电池放电时Zn转化为ZnO。该电池工作时下列说法正确的是


| A.电池工作时,电子从石墨电极经电解质溶液流向Zn电极 |
| B.该电池放电时OH-向Zn电极移动 |
| C.该电池的负极反应为Zn+H2O -2e- = ZnO+2H+ |
| D.反应前后电解质溶液的pH变大 |
锌-空气燃料电池可用作电动车动力电源,电池示意图如下,电极为金属锌和选择性催化材料,放电时,空气中的O2转化为OH-。下列说法正确的是
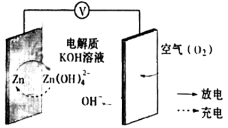

| A.充电时,电解质溶液中K+向阳极移动 |
| B.充电时,电解质溶液中c(OH-)逐渐减小 |
| C.放电时,电路中通过2 mol电子,消耗氧气1 mol |
| D.放电时,负极反应为Zn+4OH--2e-= Zn(OH) |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


