填空题 适中0.65 引用7 组卷1461
根据信息回答下列问题:
(1)如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
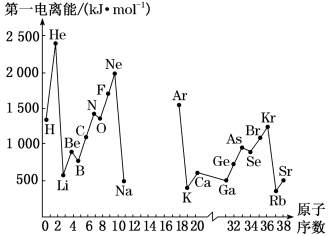
①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为
②图中Ge元素中未成对电子有
(2)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出部分元素的电负性:
元素 | Al | B | Be | C | Cl | F | Li |
电负性 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | |
元素 | Mg | N | Na | O | P | S | Si |
电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
①根据表中给出的数据,可推知元素的电负性具有的变化规律
②通过分析电负性值变化规律,确定Al元素电负性值的最小范围
③判断下列物质是离子化合物还是共价化合物:
A Li3N B PCl3 C MgCl2 D SiC
Ⅰ.属于离子化合物的是
Ⅱ.属于共价化合物的是
请设计一个实验方案证明上述所得到的结论
19-20高二下·河北唐山·期末
类题推荐
根据信息回答下列问题:
I.元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出10种元素的电负性:
已知:
i.两成键元素间电负性差值大于1.7时,形成离子键;两成键元素间电负性差值小于1.7时,形成共价键。
ii.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一。水化物M−O−H结构中,成键原子电负性差异越大,所成化学键越容易断裂,电离出OH−或H+。
(1)通过分析电负性的变化规律,确定Mg元素电负性的最小范围___________ 。
(2)判断下列物质是离子化合物还是共价化合物:
A.Li3N B.BeCl2 C.AlCl3 D.SiC
①属于离子化合物的是___________ (填字母)。
②请设计实验方案证明其为离子化合物___________ 。
(3)HClO水溶液显酸性而不显碱性的依据是___________ 。
II.元素原子的第一电离能I1随原子序数呈周期性变化,请解释:
(4)Na的第一电离能小于Li,从原子结构的角度解释其原因___________ 。
(5)S的第一电离能小于P,结合价电子排布式解释其原因___________ 。
I.元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出10种元素的电负性:
| 元素 | Al | Be | Mg | C | Cl | Na | Li | N | Si | O | H |
| 电负性 | 1.5 | 1.5 | 2.5 | 3.0 | 0.9 | 1.0 | 3.0 | 1.8 | 3.5 | 2.1 |
i.两成键元素间电负性差值大于1.7时,形成离子键;两成键元素间电负性差值小于1.7时,形成共价键。
ii.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一。水化物M−O−H结构中,成键原子电负性差异越大,所成化学键越容易断裂,电离出OH−或H+。
(1)通过分析电负性的变化规律,确定Mg元素电负性的最小范围
(2)判断下列物质是离子化合物还是共价化合物:
A.Li3N B.BeCl2 C.AlCl3 D.SiC
①属于离子化合物的是
②请设计实验方案证明其为离子化合物
(3)HClO水溶液显酸性而不显碱性的依据是
II.元素原子的第一电离能I1随原子序数呈周期性变化,请解释:
(4)Na的第一电离能小于Li,从原子结构的角度解释其原因
(5)S的第一电离能小于P,结合价电子排布式解释其原因
已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出14种元素的电负性:
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是_______ 。
(2)通过分析电负性值变化规律,确定镁元素电负性值的最小范围是_______ 。
(3)判断下列物质是离子化合物还是共价化合物:
A. B.
B. C.
C. D.
D.
属于离子化合物的是_______ ;属于共价化合物的是_______ ;请设计一个实验方案证明上述所得到的结论:_______ 。
(4)在P与 组成的化合物中,
组成的化合物中, 元素显
元素显_______ (填“正”或“负”)价,理由是_______ 。
| 元素 | B | C | F | ||||
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | N | O | P | S | |||
| 电负性 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是
(2)通过分析电负性值变化规律,确定镁元素电负性值的最小范围是
(3)判断下列物质是离子化合物还是共价化合物:
A.
属于离子化合物的是
(4)在P与
已知元素的电负性和元素的化合价一样,也是元素的一种基本性质.下面给出13种元素的电负性:
已知:两成键原子元素间电负性差值大于1.7时,形成离子键,两成键原子元素间电负性差值小于1.7时,形成共价键.
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是_____________ .
(2)通过分析电负性数值的变化规律,确定 元素电负性数值的最小范围:
元素电负性数值的最小范围:_____________ .
(3)判断下列物质是离子化合物还是共价化合物:
A. B.
B. C.
C. D.
D.
属于离子化合物的是_____________ (填字母);属于共价化合物的是___________ (填字母).请设计一个实验方案证明上述所得结论:_____________ .
元素 | |||||||
电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
元素 | |||||||
电负性 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
已知:两成键原子元素间电负性差值大于1.7时,形成离子键,两成键原子元素间电负性差值小于1.7时,形成共价键.
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是
(2)通过分析电负性数值的变化规律,确定
(3)判断下列物质是离子化合物还是共价化合物:
A.
属于离子化合物的是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


