解答题-原理综合题 适中0.65 引用1 组卷337
CO是水煤气的主要成分之一,是一种无色剧毒气体,根据信息完成下列各题。
I、已知下列热化学方程式:
2C(s) +O2(g)= 2CO(g) △H = -221 kJ/mol
C(s) + O2(g)= CO2(g) △H = -393 kJ/mol
(1)24 g单质碳在不足量的O2中燃烧时,生成等物质的量的CO和CO2气体,则和24 g单质碳完全燃烧生成CO2相比较,损失热量_________ kJ。
II、850℃时,在10 L体积不变的容器中投入2 mol CO和3 mol H2O,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g),当CO的转化率达60%时,反应达平衡。
CO2(g)+H2(g),当CO的转化率达60%时,反应达平衡。
(2)850℃时,该反应的平衡常数为_____________________ 。
(3)该条件下,将CO和H2O都改为投入2 mol, 达平衡时,H2的浓度为________ mol/L,下列情况能说明该反应一定达平衡的是__________ 。
A.CO和H2O蒸气的浓度之比不再随时间改变
B.气体的密度不再随时间改变
C.CO和CO2的浓度之比不再随时间改变
D.气体的平均摩尔质量不再随时间改变
III、(4)工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图:
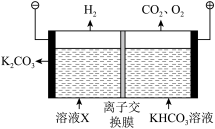
①在阳极区发生的反应包括________________ 和 H++ =CO2↑+H2O
=CO2↑+H2O
②简述 在阴极区再生的原理:
在阴极区再生的原理:_____________________________________ 。
(5)含硫各微粒(H2SO3、 和
和 )存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数ω与溶液pH的关系如图所示
)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数ω与溶液pH的关系如图所示
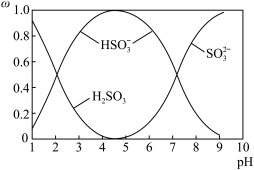
下列说法正确的是____________ (填标号)。
A. pH=7时,溶液中c( Na+)<c ( )+c(
)+c( )
)
B.由图中数据,可以估算出H2SO3的第二级电离平衡常数Ka2≈10-7
C.为获得尽可能纯的NaHSO3,应将溶液的pH控制在4~5为宜
D. pH=9时,溶液中c(OH-)=c(H+)+c( )+2c(H2SO3)
)+2c(H2SO3)
I、已知下列热化学方程式:
2C(s) +O2(g)= 2CO(g) △H = -221 kJ/mol
C(s) + O2(g)= CO2(g) △H = -393 kJ/mol
(1)24 g单质碳在不足量的O2中燃烧时,生成等物质的量的CO和CO2气体,则和24 g单质碳完全燃烧生成CO2相比较,损失热量
II、850℃时,在10 L体积不变的容器中投入2 mol CO和3 mol H2O,发生如下反应:CO(g)+H2O(g)
 CO2(g)+H2(g),当CO的转化率达60%时,反应达平衡。
CO2(g)+H2(g),当CO的转化率达60%时,反应达平衡。(2)850℃时,该反应的平衡常数为
(3)该条件下,将CO和H2O都改为投入2 mol, 达平衡时,H2的浓度为
A.CO和H2O蒸气的浓度之比不再随时间改变
B.气体的密度不再随时间改变
C.CO和CO2的浓度之比不再随时间改变
D.气体的平均摩尔质量不再随时间改变
III、(4)工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图:

①在阳极区发生的反应包括
②简述
(5)含硫各微粒(H2SO3、

下列说法正确的是
A. pH=7时,溶液中c( Na+)<c (
B.由图中数据,可以估算出H2SO3的第二级电离平衡常数Ka2≈10-7
C.为获得尽可能纯的NaHSO3,应将溶液的pH控制在4~5为宜
D. pH=9时,溶液中c(OH-)=c(H+)+c(
2020·广西南宁·模拟预测
类题推荐
CO是水煤气的主要成分之一,是一种无色剧毒气体,根据信息完成下列各题
Ⅰ、已知下列热化学方程式
2C(s) + O2(g) = 2CO(g) △H = -221kJ/mol
C(s) + O2(g) = CO2(g) △H = -393kJ/mol
24g单质碳在不足量的O2中燃烧时,生成等物质的量的CO和CO2气体,则和24g单质碳完全燃烧生成CO2相比较,损失热量_________ kJ
Ⅱ、850℃时,在10L体积不变的容器中投入2molCO和3molH2O,发生如下反应:
CO(g) + H2O(g) CO2(g) + H2(g),当CO的转化率达60%时,反应达平衡
CO2(g) + H2(g),当CO的转化率达60%时,反应达平衡
(1)850℃时,该反应的平衡常数为_________
(2)该条件下,将CO和H2O都改为投入2mol,达平衡时,H2的浓度为_________ mol/L,下列情况能说明该反应一定达平衡的是_________
Ⅲ、为防止CO使人中毒,一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇——氧化钠,其中O2-可以在固体ZASICON中自由移动,则:

(1)该原电池中通入CO的电极为_________ 极,该电极的电极反应式为___________________
(2)通空气一极的电极反应式为____________________________________
Ⅰ、已知下列热化学方程式
2C(s) + O2(g) = 2CO(g) △H = -221kJ/mol
C(s) + O2(g) = CO2(g) △H = -393kJ/mol
24g单质碳在不足量的O2中燃烧时,生成等物质的量的CO和CO2气体,则和24g单质碳完全燃烧生成CO2相比较,损失热量
Ⅱ、850℃时,在10L体积不变的容器中投入2molCO和3molH2O,发生如下反应:
CO(g) + H2O(g)
(1)850℃时,该反应的平衡常数为
(2)该条件下,将CO和H2O都改为投入2mol,达平衡时,H2的浓度为
| A.V正(CO) = V逆(CO2) |
| B.气体的密度不再随时间改变 |
| C.CO的体积分数不再随时间改变 |
| D.气体的平均摩尔质量不再随时间改变 |
Ⅲ、为防止CO使人中毒,一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇——氧化钠,其中O2-可以在固体ZASICON中自由移动,则:

(1)该原电池中通入CO的电极为
(2)通空气一极的电极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网

 CH3OH(g)
CH3OH(g)