解答题-结构与性质 较易0.85 引用1 组卷254
元素周期表是学习和研究化学的重要工具。
(1)原子序数为 1~18 的元素在元素周期表中的位置如下表所示。
①Al原子的核电荷数为____ 。②钠离子的结构示意图为____ 。
③周期表中磷元素的有关信息为 ,图中“30.97”所表示的含义是
,图中“30.97”所表示的含义是____ 。
(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价﹣物质类别”关系图。
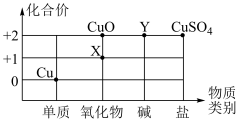
①写出物质 X 的化学式:________________ 。
②写出由物质 Y 转化为 CuSO4的化学反应方程式:_______________ 。
③氧化还原反应是化学学习中的核心概念,对氧化还原反应的定义为有化合价升降的反应,下列转化中属于氧化还原反应的是_________________ 。
A、Cu—X B、X—CuO C、CuO—Y D、Y—CuSO4
(1)原子序数为 1~18 的元素在元素周期表中的位置如下表所示。
| 第1周期 | H | He | ||||||
| 第2周期 | Li | Be | B | C | N | O | F | Ne |
| 第3周期 | Na | Mg | Al | Si | P | S | Cl | Ar |
①Al原子的核电荷数为
③周期表中磷元素的有关信息为
 ,图中“30.97”所表示的含义是
,图中“30.97”所表示的含义是(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价﹣物质类别”关系图。

①写出物质 X 的化学式:
②写出由物质 Y 转化为 CuSO4的化学反应方程式:
③氧化还原反应是化学学习中的核心概念,对氧化还原反应的定义为有化合价升降的反应,下列转化中属于氧化还原反应的是
A、Cu—X B、X—CuO C、CuO—Y D、Y—CuSO4
20-21高一上·四川雅安·开学考试
类题推荐
元素周期表是学习化学的重要工具,它隐含许多信息和规律。下表所列是六种短周期元素的原子半径及主要化合价(已知铍元素的原子半径为0.089 nm)。
(1)C元素在周期表中的位置为___ , 其离子结构示意图为: ____ 。
(2)B的最高价氧化物对应的水化物与Y的最高价氧化物对应的水化物反应的离子方程式为____ 。
(3)关于C、D 两种元素说法正确的是_________ (填序号)
a.简单离子的半径D>C b.气态氢化物的稳定性D比C强 c.最高价氧化物对应的水化物的酸性C比D强
(4)写出由A、D、X三种元素组成的某种可以消毒杀菌物质的电子式_____________ 。
(5)比较Y元素与其同族短周期元素的氢化物的稳定性_______ (填氢化物化学式),
| 元素代号 | A | B | C | D | X | Y |
| 原子半径/nm | 0.037 | 0.143 | 0.102 | 0.099 | 0.074 | 0.075 |
| 主要化合价 | +1 | +3 | +6,-2 | -1 | -2 | +5,-3 |
(1)C元素在周期表中的位置为
(2)B的最高价氧化物对应的水化物与Y的最高价氧化物对应的水化物反应的离子方程式为
(3)关于C、D 两种元素说法正确的是
a.简单离子的半径D>C b.气态氢化物的稳定性D比C强 c.最高价氧化物对应的水化物的酸性C比D强
(4)写出由A、D、X三种元素组成的某种可以消毒杀菌物质的电子式
(5)比较Y元素与其同族短周期元素的氢化物的稳定性
化学元素周期表(Periodictableofelements)是根据元素原子核电荷数从小至大排序的化学元素列表。如表是元素周期表的一部分,根据表中给出的10种元素(其中X、Y、Z分别表示某种化学元素),按要求作答。
(1)Z元素符号是___________ 。
(2)表中元素化学性质最稳定的是___________ (填元素符号)。
(3)地壳中含量最多的元素在元素周期表中的位置是___________ 。
(4)写出Na的原子结构示意图___________ 。
(5)主要用来制作高纯半导体、耐高温材料、光导纤维通信材料的元素名称是___________ 。
(6)卤族元素之一,属周期系VIIA族,在元素周期表中位于第二周期的元素是___________ 。
(7)O2与S单质相比,更难与H2化合的是___________ 。
(8)写出N元素的气态氢化物的化学式___________ ,该物质与水反应的化学方程式:___________ 。
(9)Cl2与水反应的生成物中具有漂白作用的是___________ (填化学式),写出Cl2与NaOH溶液反应的离子方程式:___________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | X | N | O | F | Y | |||
| 3 | Na | Z | Al | Si | S | Cl |
(2)表中元素化学性质最稳定的是
(3)地壳中含量最多的元素在元素周期表中的位置是
(4)写出Na的原子结构示意图
(5)主要用来制作高纯半导体、耐高温材料、光导纤维通信材料的元素名称是
(6)卤族元素之一,属周期系VIIA族,在元素周期表中位于第二周期的元素是
(7)O2与S单质相比,更难与H2化合的是
(8)写出N元素的气态氢化物的化学式
(9)Cl2与水反应的生成物中具有漂白作用的是
元素是构成我们生活的世界中一切物质的“原材料”。
(1)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。
①门捷列夫将已有元素按照相对原子质量排序,同一_________ (填“横行”或“纵列”)元素性质相似。结合表中信息,猜想第4列方框中“?=70”的问号表达的含义是______ ,第5列方框中“Te=128?”的问号表达的含义是________ 。
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量 递增呈现周期性变化,而是随着原子序数 (核电荷数)递增呈现周期性变化。其本质原因是_____ (填字母序号)。
A. 随着核电荷数递增,元素主要化合价呈现周期性变化
B. 随着核电荷数递增,原子核外电子排布呈现周期性变化
C. 随着核电荷数递增,原子半径呈现周期性变化
(2)短周期元素A、B、D、E、G、J在周期表中的位置如下:

根据上表回答问题:
①第三周期的四种元素中离子半径最小的是_________ (用元素符号填答)。
②B、D的非金属性由大到小的顺序是__________ (用元素符号填答)。
③E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为i.H++OH-=H2O、ii.___ 、iii.___ 。
④用电子式表示A2D形成过程_______________ 。
(3)元素Y的一种含氧酸化学式为 H3YO3,其结构式可表示为: 。该酸为
。该酸为______ 元酸,请写出该酸与过量氢氧化钠溶液反应的化学方程式_____ 。(用对应元素符号填答)(已知信息:氢氧原子结合成的一种原子团“—OH”叫羟基,含氧酸中只有羟基氢才可电离出 H+。)
(1)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。
| Ni=Co=59 | |||||
| H=1 | Cu=63.4 | Ag=108 | Hg=200 | ||
| Be=9.4 | Mg=24 | Zn=65.2 | Cd=112 | ||
| B=11 | Al=27.4 | ?=68 | Ur=116 | Au=198? | |
| C=12 | Si=28 | ?=70 | Sn=118 | ||
| N=14 | P=31 | As=75 | Sb=122 | Bi=210? | |
| O=16 | S=32 | Se=79.4 | Te=128? | ||
| F=19 | Cl=35.5 | Br=80 | I=127 | ||
| Li=7 | Na=23 | K=39 | Rb=85.4 | Cs=133 | Ti=204 |
| Ca=40 | Pb=207 |
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着
A. 随着核电荷数递增,元素主要化合价呈现周期性变化
B. 随着核电荷数递增,原子核外电子排布呈现周期性变化
C. 随着核电荷数递增,原子半径呈现周期性变化
(2)短周期元素A、B、D、E、G、J在周期表中的位置如下:

根据上表回答问题:
①第三周期的四种元素中离子半径最小的是
②B、D的非金属性由大到小的顺序是
③E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为i.H++OH-=H2O、ii.
④用电子式表示A2D形成过程
(3)元素Y的一种含氧酸化学式为 H3YO3,其结构式可表示为:
 。该酸为
。该酸为组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


