解答题-结构与性质 0.65 引用1 组卷47
以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵((NH4)3Fe(C6H5O7)2)。
(1)Fe 基态原子核外电子排布式为_____________ ;[ Fe(H2O)6]2+中与Fe2+配位的原子是_____ 。
(2)NH3分子中氮原子的轨道杂化类型是_______ ;与 NH 互为等电子体的一种分子为
互为等电子体的一种分子为_____ (填化学式)。
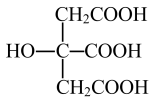
(3)柠檬酸的结构简式见图。1 mol 柠檬酸分子中碳原子与氧原子形成的σ键的数目为_______ mol。
(4)CaCN2是离子化合物,各原子均满足 8 电子稳定结构,CaCN2的电子式是_____ 。
(1)Fe 基态原子核外电子排布式为
(2)NH3分子中氮原子的轨道杂化类型是
(3)柠檬酸的结构简式见图。1 mol 柠檬酸分子中碳原子与氧原子形成的σ键的数目为

(4)CaCN2是离子化合物,各原子均满足 8 电子稳定结构,CaCN2的电子式是
19-20高三·湖北孝感·阶段练习


