解答题-工业流程题 适中0.65 引用1 组卷52
四氧化三锰既是磁性材料锰锌铁氧体(ZnaMnbFecO4,Fe元素为+3价,Zn、Mn元素化合价相同)的重要生产原料,也常被用作氮氧化物分解的催化剂。近年来对制备高品质四氧化三锰的研究越来越受到重视。以硫酸锰为原料制备四氧化三锰的工艺流程如图:
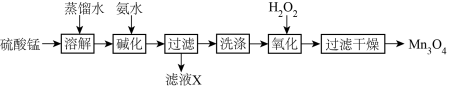
回答下列问题:
(1)“溶解”时需用玻璃棒,其作用为_____ 。
(2)“碱化”时反应离子方程式为______ 。
(3)滤液X中含有的溶质为_____ (填化学式)。
(4)简述“碱化”得到的沉淀是否洗涤干净的方法:_______ 。
(5)“氧化”时发生的化学反应方程式为_____ 。
(6)取30.2gMnSO4经上述工艺过程后,生成____ g Mn3O4(假设Mn元素不损失)。

回答下列问题:
(1)“溶解”时需用玻璃棒,其作用为
(2)“碱化”时反应离子方程式为
(3)滤液X中含有的溶质为
(4)简述“碱化”得到的沉淀是否洗涤干净的方法:
(5)“氧化”时发生的化学反应方程式为
(6)取30.2gMnSO4经上述工艺过程后,生成
19-20高二下·辽宁本溪·期末
类题推荐
四氧化三锰(Mn3O4)是电子工业的磁性材料。一种以氧化锰矿(含Mn2O3、MnOOH、Fe2O3、Al2O3、SiO2及CuO等)为原料制备Mn3O4的工艺流程如图:
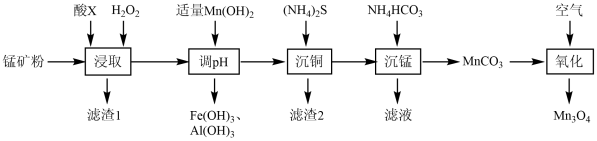
I.常温下,溶液中金属离子开始沉淀和沉淀完全的pH如表:
II.常温下,Ksp[Cu(OH)2]=2×10-20。
回答下列问题:
(1)①“浸取”过程中加入的酸X是_____ (填字母)。原因是_____ 。
A.硫酸 B.盐酸 C.硝酸
②加入H2O2的作用是_____ 。
(2)加入适量Mn(OH)2以除去溶液中的铁、铝元素,此时溶液中c(Cu2+)=2×10-3mol·L-1,则调节pH的范围为_____ 。
(3)“滤渣2”的主要成分是_____ (填化学式)。
(4)“沉锰”时发生反应的离子方程式为_____ ,“滤液”中溶质的主要成分是_____ (填化学式)。

I.常温下,溶液中金属离子开始沉淀和沉淀完全的pH如表:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ |
| 开始沉淀的pH | 7.8 | 6.5 | 1.5 | 3.3 |
| 沉淀完全的pH | 10.4 | 9.7 | 3.2 | 5.2 |
回答下列问题:
(1)①“浸取”过程中加入的酸X是
A.硫酸 B.盐酸 C.硝酸
②加入H2O2的作用是
(2)加入适量Mn(OH)2以除去溶液中的铁、铝元素,此时溶液中c(Cu2+)=2×10-3mol·L-1,则调节pH的范围为
(3)“滤渣2”的主要成分是
(4)“沉锰”时发生反应的离子方程式为
四氧化三锰是一种重要的化工产品,主要用于电子工业,一种以软锰矿(主要成分为MnO2,杂质金属元素为Fe、Mg、Al等)、硫铁矿(主要成分为FeS2,杂质主要为SiO2等)为原料制备Mn3O4的工艺流程如图。
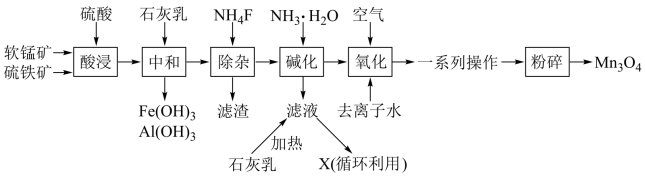
回答下列问题:
(1)流程中多次用到了过滤操作,该操作所用的玻璃仪器有普通漏斗、烧杯、___ 。
(2)为了提高“酸浸”时的浸取速率,可采取的措施有___ (任写一种);“酸浸”时生成Fe2(SO4)3和MnSO4的化学方程式为___ 。
(3)常温时部分金属离子在溶液中完全沉淀时的pH如表所示:
则“中和”时调节溶液pH的最小值为___ (填整数),“除杂”时,滤渣的主要成分为___ (填化学式)。
(4)循环利用的物质X为___ (填化学式),生成该物质的离子方程式为___ ;证明Mn(OH)2已洗涤干净的操作为___ 。
(5)“一系列操作”包括___ 。

回答下列问题:
(1)流程中多次用到了过滤操作,该操作所用的玻璃仪器有普通漏斗、烧杯、
(2)为了提高“酸浸”时的浸取速率,可采取的措施有
(3)常温时部分金属离子在溶液中完全沉淀时的pH如表所示:
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ | Mg2+ |
| 完全沉淀时的pH | 9.7 | 3.2 | 4.7 | 10.4 | 12.4 |
则“中和”时调节溶液pH的最小值为
(4)循环利用的物质X为
(5)“一系列操作”包括
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



