计算题 较易0.85 引用1 组卷380
工业上用化学气相沉积法制备氮化硅,其反应:3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g) △H<0。某温度和压强条件下,分别将0.3mol SiCl4(g)、0.2mol N2(g)、0.6mol H2(g)充入2L密闭容器内,进行上述反应,5min所得Si3N4(s)的质量是5.60g(Si3N4的摩尔质量为140g/mol)。
Si3N4(s)+12HCl(g) △H<0。某温度和压强条件下,分别将0.3mol SiCl4(g)、0.2mol N2(g)、0.6mol H2(g)充入2L密闭容器内,进行上述反应,5min所得Si3N4(s)的质量是5.60g(Si3N4的摩尔质量为140g/mol)。
(1)H2的平均反应速率是______ 。
(2)5min时容器内N2的浓度是______ 。
(3)5min时容器内HCl的物质的量分数是______ 。
(4)5min时SiCl4(g)的转化率是______ 。
(5)5min时容器内的压强是原来的______ 倍。
(1)H2的平均反应速率是
(2)5min时容器内N2的浓度是
(3)5min时容器内HCl的物质的量分数是
(4)5min时SiCl4(g)的转化率是
(5)5min时容器内的压强是原来的
2020·北京·模拟预测
类题推荐
工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g) ΔH<0
Si3N4(s)+12HCl(g) ΔH<0
某温度和压强条件下,分别将1.25mol SiCl4(g)、1.0mol N2(g)、10.5mol H2(g)充入20L密闭容器内,进行上述反应,5min达到平衡状态,所得Si3N4(s)的质量是35.0g.已知:
(1)计算该反应的ΔH=_______________
(2)H2的平均反应速率是
(3)平衡时容器内N2的浓度是
(4)SiCl4(g)的转化率是 %
(5)下图为合成Si3N4反应中SiCl4平衡转化率与温度、压强的关系(n(SiCl4)、n(N2)、n(H2)仍按1.25 mol SiCl4(g)、1.0 mol N2(g)、10.5mol H2(g)投入)

上图中压强最大的是_____(P1、P2、P3、P4),列式计算合成Si3N4反应在图中A点的分压平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,图中P2=13MPa)
3SiCl4(g)+2N2(g)+6H2(g)
 Si3N4(s)+12HCl(g) ΔH<0
Si3N4(s)+12HCl(g) ΔH<0某温度和压强条件下,分别将1.25mol SiCl4(g)、1.0mol N2(g)、10.5mol H2(g)充入20L密闭容器内,进行上述反应,5min达到平衡状态,所得Si3N4(s)的质量是35.0g.已知:
| 化学键 | Si-Cl | N≡N | H-H | Si-N | H-Cl |
| 键能(KJ/mol) | a | b | c | d | e |
(1)计算该反应的ΔH=_______________
(2)H2的平均反应速率是
(3)平衡时容器内N2的浓度是
(4)SiCl4(g)的转化率是 %
(5)下图为合成Si3N4反应中SiCl4平衡转化率与温度、压强的关系(n(SiCl4)、n(N2)、n(H2)仍按1.25 mol SiCl4(g)、1.0 mol N2(g)、10.5mol H2(g)投入)

上图中压强最大的是_____(P1、P2、P3、P4),列式计算合成Si3N4反应在图中A点的分压平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,图中P2=13MPa)
工业制备氮化硅的反应为:3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g) ΔH<0,将0.3 mol SiCl4和一定量 N2、H2投入2 L反应容器,只改变温度条件测得Si3N4的质量变化如下表:
Si3N4(s)+12HCl(g) ΔH<0,将0.3 mol SiCl4和一定量 N2、H2投入2 L反应容器,只改变温度条件测得Si3N4的质量变化如下表:
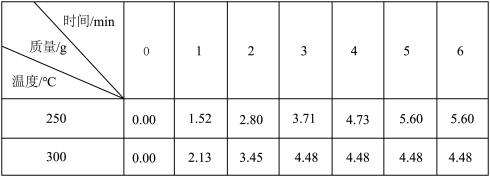
下列说法正确的是( )

下列说法正确的是( )
| A.250 ℃,前2 min, Si3N4 的平均反应速率为0.02 mol·L-1·min-1 |
| B.反应达到平衡时, 两种温度下 N2和 H2的转化率之比相同 |
| C.达到平衡前,300 ℃条件的反应速率比250 ℃快; 平衡后,300 ℃比250 ℃慢 |
| D.反应达到平衡时, 两种条件下反应放出的热量一样多 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


