单选题 适中0.65 引用1 组卷92
用VB2-空气电池电解硝酸银溶液(a、b、c均为惰性电极)装置如图所示。VB2电极的反应式为:2VB2+22OH--22e-=V2O5+2B2O3+11H2O,当外电路中通过0.04mol电子时,B装置内共收集到0.448 L气体(标准状况),则下列说法错误的是
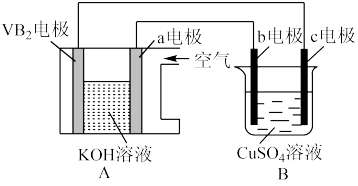

| A.原电池工作时总反应为:4VB2+11O2=4B2O3+2V2O5 |
| B.b电极为阳极,发生氧化反应 |
| C.电解过程中,c电极表面先有固体物质析出,后有气泡产生 |
| D.若B装置内的液体体积为100 mL(忽略体积变化),则硝酸银溶液的物质的量浓度为0.4mol•L-1 |
19-20高一下·山东威海·期末
类题推荐
碱性硼化钒(VB2)—空气电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
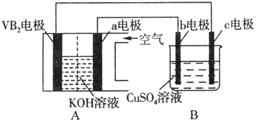

| A.VB2电极发生的电极反应为:2VB2 + 11H2O - 22e- = V2O5 + 2B2O3 + 22H+ |
| B.外电路中电子由c电极流向VB2电极 |
| C.电解过程中,c电极表面先有红色物质析出,后有气泡产生 |
| D.若B装置内的液体体积为100 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L |
碱性硼化钒(VB2)-空气电池工作时反应为:4VB2+11O2 = 4B2O3+2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )
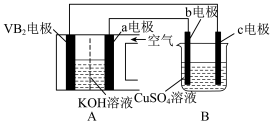

| A.VB2电极发生的电极反应为:2VB2+11H2O-22e- = V2O5+2B2O3+22H+ |
| B.外电路中电子由c电极流向VB2电极 |
| C.电解过程中,c电极表面先有红色物质析出,然后有气泡产生 |
| D.若B装置内的液体体积为100 mL,则CuSO4溶液的物质的量浓度为0.2mol/L |
碱性硼化钒(VB2)—空气电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5。用该电池为电源, 选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是


| A.电解过程中,c电极表面先有红色物质析出,后有气泡产生 |
| B.外电路中电子由c电极流向VB2电极 |
| C.VB2电极发生的电极反应为: 2VB2 + 11H2O - 22e- = V2O5 + 2B2O3 + 22H+ |
| D.若B装置内的液体体积为100 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


