解答题-无机推断题 适中0.65 引用1 组卷129
1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。
(1)已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下均呈气态;Y的原子最外层电子数是其电子层数的2倍;M与X同族;Z、G分别是地壳中含量最高的非金属元素和金属元素。回答下列问题:
①Y、Z、M、G四种元素的原子半径由大到小的顺序是______ (用元素符号表示)。
②用电子式表示M2Z的形成过程_______ 。
③上述元素的最高价氧化物对应的水化物中,酸性最强的水化物是_____ (写化学式)。
④GQ3溶液与过量的MZX溶液反应的化学方程式为________ 。
⑤常温下,不能与G的单质发生反应的是______ (填序号)。
a.CuSO4溶液b.NaOH溶液c.Na2CO3固体d.氧化铁e.浓硝酸
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置_______ 。
②关于铷的下列说法中不正确的是________ (填序号)。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
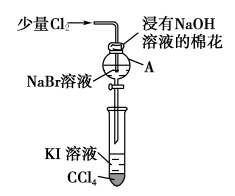
①棉花中浸有NaOH溶液的作用是___________________ (用离子方程式表示)。
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到_______________ ;该实验必须控制氯气的加入量,否则得不出溴的非金属性比碘强的结论,理由是_________________ 。
(1)已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下均呈气态;Y的原子最外层电子数是其电子层数的2倍;M与X同族;Z、G分别是地壳中含量最高的非金属元素和金属元素。回答下列问题:
①Y、Z、M、G四种元素的原子半径由大到小的顺序是
②用电子式表示M2Z的形成过程
③上述元素的最高价氧化物对应的水化物中,酸性最强的水化物是
④GQ3溶液与过量的MZX溶液反应的化学方程式为
⑤常温下,不能与G的单质发生反应的是
a.CuSO4溶液b.NaOH溶液c.Na2CO3固体d.氧化铁e.浓硝酸
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置
②关于铷的下列说法中不正确的是
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:

①棉花中浸有NaOH溶液的作用是
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到
19-20高一下·山东临沂·期末
类题推荐
1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一、下表是元素周期表的一部分
(1)元素④的过氧化物的电子式为___________ ,其最高价氧化物对应的水化物含有的化学键类型为___________ ,⑩元素最高价氧化物对应的水化物的化学式是___________ 。
(2)元素①、②、③的简单氢化物的稳定性最强的是___________ ,④、⑤最高价氧化物对应的水化物碱性更强的是___________ ,④、⑤、⑧、⑨的简单离子半径由大到小的顺序___________ (均用化学式或离子符号表示)。
(3)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。铷在元素周期表中的位置为___________ 。下列关于铷的下列说法中不正确的是___________ (填序号)。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 二 | ① | ② | ③ | ||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ |
(2)元素①、②、③的简单氢化物的稳定性最强的是
(3)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。铷在元素周期表中的位置为
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。元素周期表与元素周期律在化学学习研究中有很重要的作用。
(1)下表是元素周期表的一部分
i.元素④的过氧化物的电子式为______ ,其最高价氧化物对应的水化物含有的化学键类型为______ ,⑩元素最高价氧化物对应的水化物的化学式是______ 。
ii.元素①、②、③的简单氢化物的稳定性最强的是______ (用化学式表示,下同),②、⑧简单氢化物熔点高的是______ ,④、⑤最高价氧化物的水化物碱性更强的是______ ,④、⑤、⑧、⑨的简单离子半径由大到小的顺序______ 。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置______ 。
ii.关于铷的下列说法中不正确的是______ (填序号)。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(1)下表是元素周期表的一部分
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 四 | ⑩ |
i.元素④的过氧化物的电子式为
ii.元素①、②、③的简单氢化物的稳定性最强的是
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置
ii.关于铷的下列说法中不正确的是
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网