解答题-结构与性质 0.65 引用1 组卷35
金属氮化物具有高熔点、高硬度、高化学稳定性以及良好的导热、导电性,目前已经广泛应用于磁学、电子工业 、耐高温结构陶瓷等领域 。回答下列问题
(1)下列不同状态的氮原子其能量最高的是________ (填字母),基态氮原子处于最高能级的电子其电子云轮廓图形状为________
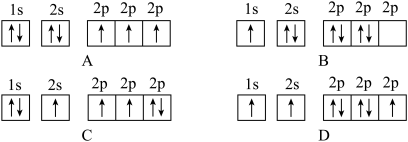
(2)第一电离能I1(N)______ (填“> ”“< ”或“=”)I1(P),其原因是_____________ 。
(3)A和B两种金属的含氮化合物的结构如图所示:
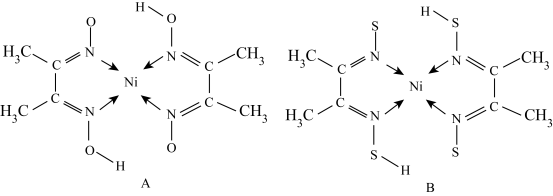
①基态 Ni 原子的核外电子排布式为[ Ar]________________ 。
②物质A 中碳原子的杂化方式为__________________ 。
③A的熔点高于 B 的,具主要原因是_______ 。
④B中含有的化学键类型有_____________ (填字母)。
a.金属键 b. σ建
c.π键 d. 配位键
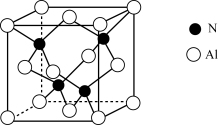
(4)氮化铝晶胞如图所示。氮原子的配位数为_______ ,每个铝原子周围紧邻__________ 个铝原子;已知立方氮化铝晶体密度为ρg• cm-3,晶胞中最近的两个铝原子之间的距离为___ pm(列出计算式即可,阿伏加 德罗常数为6. 02×1023mol -1)。
(1)下列不同状态的氮原子其能量最高的是

(2)第一电离能I1(N)
(3)A和B两种金属的含氮化合物的结构如图所示:

①基态 Ni 原子的核外电子排布式为[ Ar]
②物质A 中碳原子的杂化方式为
③A的熔点高于 B 的,具主要原因是
④B中含有的化学键类型有
a.金属键 b. σ建
c.π键 d. 配位键
(4)氮化铝晶胞如图所示。氮原子的配位数为

19-20高二下·河南·阶段练习


