解答题-结构与性质 适中0.65 引用1 组卷58
亚铁氰化钾(K4[Fe(CN)6])又称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝)+3KCl,回答问题:
(1)写出基态Fe2+的核外电子排布式__ 。
(2)K4[Fe(CN)6]中的作用力除共价键外,还有__ 和__ 。1molK4[Fe(CN)6]含有σ键为__ mol。
(3)黄血盐中N原子的杂化方式为__ ;C、N、O的第一电离能由大到小的排序为__ ,电负性由大到小的排序为__ 。
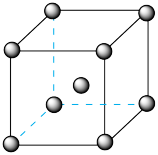
(4)Fe、Na、K的晶体结构如图所示:
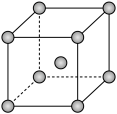
①钠的熔点比钾更高,原因是__ 。
②Fe原子半径是rcm,阿伏加 德罗常数为NA,铁的相对原子质量为a,则铁单质的密度是__ g/cm3。
(1)写出基态Fe2+的核外电子排布式
(2)K4[Fe(CN)6]中的作用力除共价键外,还有
(3)黄血盐中N原子的杂化方式为
(4)Fe、Na、K的晶体结构如图所示:

①钠的熔点比钾更高,原因是
②Fe原子半径是rcm,阿伏加 德罗常数为NA,铁的相对原子质量为a,则铁单质的密度是
19-20高二下·辽宁大连·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网