解答题-原理综合题 适中0.65 引用23 组卷11117
探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.

Ⅱ.

Ⅲ.

回答下列问题:
(1)
_________  。
。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为ɑ mol,CO为b mol,此时H2(g)的浓度为__________ mol﹒L-1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为___________ 。
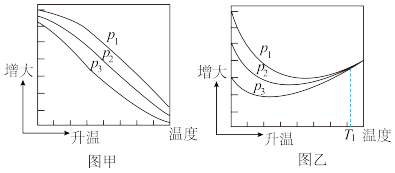
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
CH3OH的平衡产率=
其中纵坐标表示CO2平衡转化率的是图___________ (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为___________ ;图乙中T1温度时,三条曲线几乎交于一点的原因是___________ 。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_________ (填标号)。
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
Ⅰ.
Ⅱ.
Ⅲ.
回答下列问题:
(1)
(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为ɑ mol,CO为b mol,此时H2(g)的浓度为
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
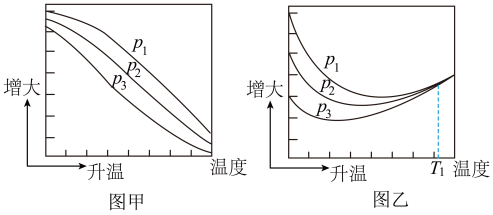
CH3OH的平衡产率=
其中纵坐标表示CO2平衡转化率的是图
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
2020·山东·高考真题
类题推荐
探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH1=-49.5kJ·mol-1
CH3OH(g)+H2O(g)ΔH1=-49.5kJ·mol-1
Ⅱ.CO(g)+2H2(g) CH3OH(g)ΔH2=-90.4kJ·mol-1
CH3OH(g)ΔH2=-90.4kJ·mol-1
Ⅲ.CO2(g)+H2(g) CO(g)+H2O(g)ΔH3
CO(g)+H2O(g)ΔH3
回答下列问题:
(1)ΔH3=___ kJ·mol-1。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中CH3OH(g)为xmol,CO为ymol,此时H2O(g)的浓度为___ mol·L-1(用含x、y、V的代数式表示,下同),反应Ⅲ的平衡常数为___ 。
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。

已知:CO2的平衡转化率= ×100%
×100%
CH3OH的平衡产率= ×100%
×100%
①其中纵坐标表示CO2平衡转化率的是图___ (填“甲”或“乙”)。
②压强p1、p2、p3由大到小的顺序为___ 。
③图乙中T1温度时,三条曲线几乎交于一点的原因是___ 。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为___ (填标号)。
(5)在T1温度时,将1.00molCO2和3.00molH2充入体积为1.00L的恒容密闭容器中,容器起始压强为p0,仅进行反应I。
①充分反应达到平衡后,若CO2转化率为x,则容器的压强与起始压强之比为___ (用x表示)。
②若经过30h反应达到平衡,平衡后,混合气体物质的量为3.00mol,则该过程中H2的平均反应速率为___ (保留三位有效数字)。
③平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数.写出上述反应压力平衡常数Kp为___ (用p0表示,并化简)。
Ⅰ.CO2(g)+3H2(g)
Ⅱ.CO(g)+2H2(g)
Ⅲ.CO2(g)+H2(g)
回答下列问题:
(1)ΔH3=
(2)一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中CH3OH(g)为xmol,CO为ymol,此时H2O(g)的浓度为
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。

已知:CO2的平衡转化率=
CH3OH的平衡产率=
①其中纵坐标表示CO2平衡转化率的是图
②压强p1、p2、p3由大到小的顺序为
③图乙中T1温度时,三条曲线几乎交于一点的原因是
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为
| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
①充分反应达到平衡后,若CO2转化率为x,则容器的压强与起始压强之比为
②若经过30h反应达到平衡,平衡后,混合气体物质的量为3.00mol,则该过程中H2的平均反应速率为
③平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数.写出上述反应压力平衡常数Kp为
(一)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。
以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=-49.5kJ•mol-1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g)△H2
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g)△H3>0
已知CO(g)、H2(g)、CH3OH(g)的标准燃烧热分别为-285.8kJ•mol-1,-283.0kJ•mol-1,-761.0kJ•mol-1回答下列问题:
(1)△H2=___ kJ•mol-1。
(2)一定条件下,向体积一定的恒容密闭容器中通入1mol CO2和3mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,此时H2O(g)的物质的量为___ mol(用含a,b的代数式表示,下同),反应Ⅲ的平衡常数为___ 。
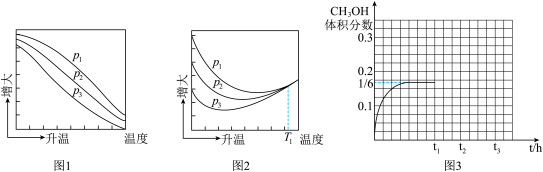
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CH3OH的平衡产率(图1)和CO2的平衡转化率(图2)随温度的变化关系如图所示。
已知:CO2的平衡转化率= ×100%
×100%
CH3OH的平衡产率= ×100%
×100%
① 图1中,一定压强下,CH3OH的平衡产率随温度升高而下降的原因是___________________________________ 。
② 图1中,压强p1、p2、p3由大到小的顺序为___ 。
③ 图2中T1温度时,三条曲线几乎交于一点的原因是____________________________________________________ 。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为___ 。
(二)若只考虑反应Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=-49.5kJ•mol-1一定条件下,向体积一定的恒容密闭容器中通入1mol CO2和3mol H2发生上述反应,得到CH3OH(g)体积分数与时间的关系如图3所示。保持其它条件不变,t1时再向容器中充入通入1mol CO2和3mol H2,t2时再次达到平衡。
(5)请画出t1-t3时间范围内CH3OH体积分数随时间的变化曲线___ 。

以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=-49.5kJ•mol-1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g)△H2
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g)△H3>0
已知CO(g)、H2(g)、CH3OH(g)的标准燃烧热分别为-285.8kJ•mol-1,-283.0kJ•mol-1,-761.0kJ•mol-1回答下列问题:
(1)△H2=
(2)一定条件下,向体积一定的恒容密闭容器中通入1mol CO2和3mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,此时H2O(g)的物质的量为
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CH3OH的平衡产率(图1)和CO2的平衡转化率(图2)随温度的变化关系如图所示。
已知:CO2的平衡转化率=
CH3OH的平衡产率=
① 图1中,一定压强下,CH3OH的平衡产率随温度升高而下降的原因是
② 图1中,压强p1、p2、p3由大到小的顺序为
③ 图2中T1温度时,三条曲线几乎交于一点的原因是
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为___ 。
| A.低温、高压 |
| B.高温、低压 |
| C.低温、低压 |
| D.高温、高压 |
(二)若只考虑反应Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=-49.5kJ•mol-1一定条件下,向体积一定的恒容密闭容器中通入1mol CO2和3mol H2发生上述反应,得到CH3OH(g)体积分数与时间的关系如图3所示。保持其它条件不变,t1时再向容器中充入通入1mol CO2和3mol H2,t2时再次达到平衡。
(5)请画出t1-t3时间范围内CH3OH体积分数随时间的变化曲线
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网