单选题 适中0.65 引用1 组卷112
高铁酸钾(K2FeO4)是一种集氧化、杀菌、脱色、除臭的新型高效水处理剂,工业上可通过 Fe(NO3)3与NaClO在强碱性介质中反应生成紫红色高铁酸盐溶液,其对应的工业流程如图所示。有关说法正确的是
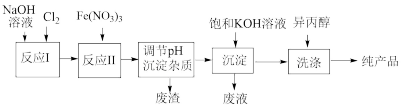

| A.K2FeO4能够作为净水剂的原因,在于其氧化产物能够水解生成氢氧化铁胶体 |
| B.反应II的离子方程式为 3ClO−+5H2O+2Fe3+=2 |
| C.向Na2FeO4中加入饱和KOH 溶液,析出K2FeO4沉淀,说明K2FeO4的溶解度比Na2FeO4大 |
| D.洗涤粗品时选用异丙醇而不用水,可以减少K2FeO4的溶解损失 |
19-20高二下·北京·阶段练习
类题推荐
高铁酸盐在能源、环保等方面有着广泛的用途,高铁酸钾在异丙醇中溶解度非常小。湿法、干法制备高铁酸盐的原理如下表所示。
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如图所示:
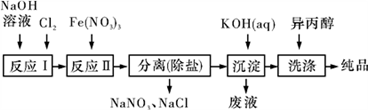
①洗涤粗品时选用异丙醇而不用水的理由是__________________________________ 。
②反应Ⅱ的离子方程式为__________________________________________________ 。
(2)由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠中加入饱和KOH溶液,即可析出高铁酸钾,析出后溶液中c(K+)<c(Na+)。由以上信息可知______ (填字母)。
A.高铁酸钾的溶解度比高铁酸钠大 B.Ksp(K2FeO4)<Ksp(Na2FeO4)
(3)干法制备K2FeO4的反应中氧化剂与还原剂的物质的量之比为__________________ 。
(4)锌-锰碱性电池以KOH溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+2H2O(l)═Zn(OH)2(s)+2MnOOH(s)。Zn--K2FeO4 也可以组成碱性电池,与 Zn--MnO2电池类似。K2FeO4在电池中作正极材料,其电极反应式为__________________________________________________________ ,
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如图所示:

①洗涤粗品时选用异丙醇而不用水的理由是
②反应Ⅱ的离子方程式为
(2)由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠中加入饱和KOH溶液,即可析出高铁酸钾,析出后溶液中c(K+)<c(Na+)。由以上信息可知
A.高铁酸钾的溶解度比高铁酸钠大 B.Ksp(K2FeO4)<Ksp(Na2FeO4)
(3)干法制备K2FeO4的反应中氧化剂与还原剂的物质的量之比为
(4)锌-锰碱性电池以KOH溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+2H2O(l)═Zn(OH)2(s)+2MnOOH(s)。Zn--K2FeO4 也可以组成碱性电池,与 Zn--MnO2电池类似。K2FeO4在电池中作正极材料,其电极反应式为
高铁酸钾(K2FeO4)是一种新型、高效的水处理剂,工业上通常用下列反应先制得高铁酸钠:2FeC13+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O,然后在某低温下,在高铁酸钠溶液中加KOH固体至饱和就可析出高铁酸钾。下列说法不正确的是
| A.NaClO在反应中作氧化剂 |
| B.制取高铁酸钠时,每生成1mol Na2FeO4,反应中共有6mol电子转移 |
| C.高铁酸钾在低温下的溶解度比高铁酸钠的溶解度小 |
| D.K2FeO4能消毒杀菌,其还原产物水解生成的Fe(OH)3胶体能吸附水中的悬浮杂质 |
高铁酸钾(K2FeO4)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓KOH溶液,能溶于水,且能与水反应放出氧气,并生成Fe(OH)3胶体,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于Cl2、KMnO4等。工业上湿法制备K2FeO4的流程如下:
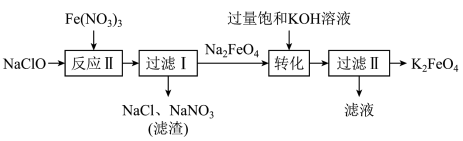
下列关于K2FeO4的工业湿法制备工艺,说法正确的是

下列关于K2FeO4的工业湿法制备工艺,说法正确的是
| A.“反应Ⅱ”中,氧化剂和还原剂的物质的量之比为2:3 |
| B.“过滤I”所得滤液中大量存在的离子有:Na+、Fe2+、Cl-、FeO |
| C.“转化”时,反应能进行说明该条件下K2FeO4的溶解度小于Na2FeO4 |
| D.“过滤Ⅱ”所得滤液进行焰色反应时火焰呈黄色,说明滤液中不含有KOH |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


