解答题-结构与性质 适中0.65 引用1 组卷93
化学上常利用周期表中同族元素的相似性与递变性研究元素的原子结构和性质。回答下列问题:
(1)现代化学中,常利用_____ 特征谱线来鉴定元素。
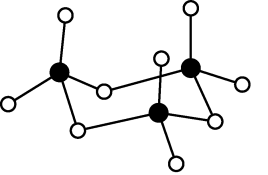
(2)氧族元素中,氧、硫、硒三元素的第一电离能由大到小的顺序为_____ (用元素符号回答),气态SO3为单分子状态,其分子空间构型为_____ 。若SO3的三聚体(SO3)3的环状结构如图所示,则该结构中S原子的杂化轨道类型为_____ 。
(3)卤族元素的氢化物中,H﹣F键的键能>H﹣Cl键的键能>H﹣Br键的键能,原因是_____ 。
(4)铁、钴、镍同处在元素周期表中_____ 族,它们的阳离子易形成各种配合物,已知:磁矩u= ,n为中心原子或离子的单电子数,实验测得配合物[Co(NH3)4Cl2]Cl中u=0,则其中心粒子的化合价为
,n为中心原子或离子的单电子数,实验测得配合物[Co(NH3)4Cl2]Cl中u=0,则其中心粒子的化合价为_____ ,其价电子排布图为_____ 。
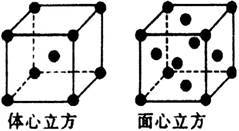
(5)已知:铜晶体为面心立方最密堆积,铜原子半径为rpm,阿伏加 德罗常数用NA表示,则铜晶体密度的计算式为_____ 。
(1)现代化学中,常利用
(2)氧族元素中,氧、硫、硒三元素的第一电离能由大到小的顺序为
(3)卤族元素的氢化物中,H﹣F键的键能>H﹣Cl键的键能>H﹣Br键的键能,原因是
(4)铁、钴、镍同处在元素周期表中
(5)已知:铜晶体为面心立方最密堆积,铜原子半径为rpm,阿伏加 德罗常数用NA表示,则铜晶体密度的计算式为

18-19高二下·云南昆明·期末
类题推荐
[化学——选修3:物质结构与性质]太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质。
(1)基态硅原子的价电子排布图:_________ 。
(2)硒和硫同为VIA族元素,与其相邻的元素有砷和溴,则三种元素的第二电离能由小到大的顺序为____ 。(用I2X表示)
(3)气态SeO3分子的杂化类型为_______ ,与SeO3互为等电子体的一种阴离子为_______ (填化学式)。
(4)胆矾CuSO4·5H2O可写成[Cu(H2O) 4]SO4·H2O,其结构示意图如下:
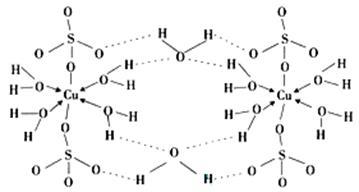
胆矾中含有的粒子间作用力是________ (填序号)。
(5)在硫酸铜溶液中加入过量KCN,生成配合物K 2[Cu(CN)4],该配合物属于_________ 晶体,已知CN-与N2为等电子体,指出1molCN-中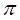 键的数目为
键的数目为___________ 。
(6)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中金原子位于顶点,铜原子位于面心,则该合金中铜原子(Cu)与金原子(Au)个数比为________ ;若该晶体的晶胞棱长为a nm,则该合金密度为____ g/cm3。(列出计算式,不要求计算结果,阿伏加德罗常数的值为NA)
(1)基态硅原子的价电子排布图:
(2)硒和硫同为VIA族元素,与其相邻的元素有砷和溴,则三种元素的第二电离能由小到大的顺序为
(3)气态SeO3分子的杂化类型为
(4)胆矾CuSO4·5H2O可写成[Cu(H2O) 4]SO4·H2O,其结构示意图如下:

胆矾中含有的粒子间作用力是
| A.离子键 | B.极性键 | C.金属键 | D.配位键 E.氢键 F.非极性键 |
(5)在硫酸铜溶液中加入过量KCN,生成配合物K 2[Cu(CN)4],该配合物属于
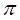 键的数目为
键的数目为(6)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中金原子位于顶点,铜原子位于面心,则该合金中铜原子(Cu)与金原子(Au)个数比为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网