单选题 适中0.65 引用1 组卷71
下列实验事实不能用平衡移动原理解释的是
| A.升高温度水的离子积增大 | B.镁条与氯化铵溶液反应生成氢气 |
| C.制备 H2 时用粗锌比纯锌的速率快 | D.压缩 NO2 的体积,气体的颜色先加深后逐渐变浅 |
19-20高二下·北京海淀·期末
类题推荐
2SO2(g)+O2(g)  2SO3(g) △H=-196.6kJ/mol是制备硫酸的重要反应。叙述不正确的是
2SO3(g) △H=-196.6kJ/mol是制备硫酸的重要反应。叙述不正确的是
 2SO3(g) △H=-196.6kJ/mol是制备硫酸的重要反应。叙述不正确的是
2SO3(g) △H=-196.6kJ/mol是制备硫酸的重要反应。叙述不正确的是| A.反应达到平衡状态后,SO3(g)浓度保持不变 | B.催化剂V2O5能够加快反应速率 |
| C.增加O2的浓度将提高SO2的转化率 | D.降低温度可以缩短反应达到平衡的时间 |
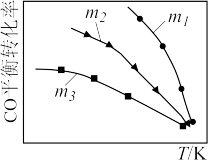
利用反应 ,可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比
,可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是

| A.该反应的 |
| B.投料比: |
| C.汽车排气管中的催化剂可提高NO的平衡转化率 |
| D.若m=2,反应达平衡时,NO的转化率为40%,则 |
甲烷催化双重整制备合成气(CO和H2)包括了水蒸气重整(反应I)和二氧化碳重整(反应Ⅱ)两个反应。在P=3.2×106pa下,向密闭容器中按n(CH4)∶n(H2O)∶n(CO2)=5∶4∶2通入混合气,发生反应:(Ea表示反应中基元反应的最大活化能)
反应I:CH4(g) + H2O(g) =CO(g) + 3H2(g) ΔH1 = +206.2kJ·mol-1Ea1 = 240.1kJ·mol-1
反应Ⅱ:CH4(g) + CO2(g) =2CO(g) + 2H2(g) ΔH2 = +247.0kJ·mol-1 Ea2 = 577.6kJ·mol-1
副反应:CH4(g) =C(s) + 2H2(g)
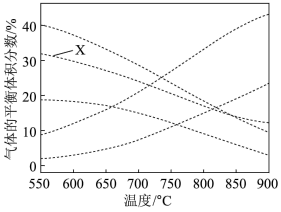
重整体系中,各气体的平衡体积分数随温度的变化如图所示。下列说法正确的是
反应I:CH4(g) + H2O(g) =CO(g) + 3H2(g) ΔH1 = +206.2kJ·mol-1Ea1 = 240.1kJ·mol-1
反应Ⅱ:CH4(g) + CO2(g) =2CO(g) + 2H2(g) ΔH2 = +247.0kJ·mol-1 Ea2 = 577.6kJ·mol-1
副反应:CH4(g) =C(s) + 2H2(g)
重整体系中,各气体的平衡体积分数随温度的变化如图所示。下列说法正确的是

| A.CO(g) + H2O(g) = CO2(g) + H2(g) ΔH = +40.8kJ·mol-1 |
| B.图中曲线X表示平衡时CH4的体积分数随温度的变化 |
| C.其他条件不变,550~900℃范围内升高温度,平衡时n(H2)/n(CO) 比值不断增大 |
| D.温度过高,由于副反应发生,会导致甲烷双重整反应速率迅速下降 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


