解答题-原理综合题 较难0.4 引用1 组卷107
氮的化合物既是重要的工业原料,也是主要的大气污染来源,研究氮的化合物的反应具有重要意义。
(Ⅰ)消除氮氧化物有多种方法。
(1)NH3催化还原法:原理如图所示
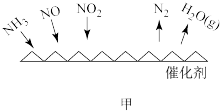
①若烟气中 c(NO2):c(NO)=1∶1,发生如图甲所示的脱氮反应时,反应过程中转移1.5mol电子时放出的热量为 113.8 kJ,则发生该脱氮反应的热化学方程式为___________ 。
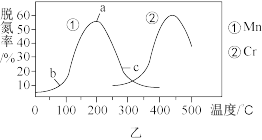
②图乙是在一定时间内,使用不同催化剂 Mn 和 Cr 在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应温度分别为_________ ;使用 Mn 作催化剂时,脱氮率 b~a 段呈现如图变化的可能原因是__________ 。
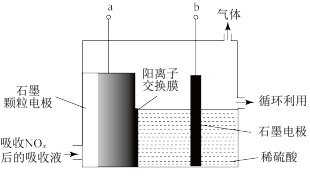
(2)直接电解吸收也是脱硝的一种方法。用6%的稀硝酸吸收NOx生成亚硝酸,再将吸收液导入电解槽电解,使之转化为硝酸。电解装置如右下图所示。阳极的电极反应式为__________ 。
(Ⅱ)氨是重要的化工原料,工业合成氨有重要现实意义。
(1)在773K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中发生反应生成NH3,气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。
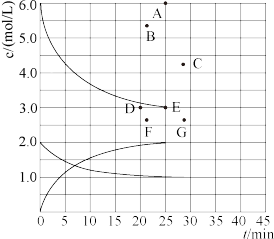
①下列能说明反应达到平衡状态的是____ (选填字母)。
a.v正(N2)=3v逆(H2) b.体系压强不变
c.气体平均相对分子质量不变 d.气体密度不变
②在此温度下,若起始充入4.00mol N2和12.00mol H2,则反应刚达到平衡时,表示 c(H2)~t的曲线上相应的点为___ (选填字母)。
(2)在373 K时,向体积为2L的恒容真空容器中充入0.40mol NO2,发生如下反应:2NO2(g)⇌N2O4(g) ∆H=-56.9kJ‧mol-1,测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
①计算0~20min时,v(N2O4)=____________ 。
②已知该反应v正(NO2)=k1‧c2(NO2),v逆(N2O4)=k2‧c(N2O4),其中k1、k2为速率常数,则373K时, =
=_________ ;改变温度至T1时,k1=k2,则T1_______ 373K(填“>”“<”或“=”)。
(Ⅰ)消除氮氧化物有多种方法。
(1)NH3催化还原法:原理如图所示


①若烟气中 c(NO2):c(NO)=1∶1,发生如图甲所示的脱氮反应时,反应过程中转移1.5mol电子时放出的热量为 113.8 kJ,则发生该脱氮反应的热化学方程式为
②图乙是在一定时间内,使用不同催化剂 Mn 和 Cr 在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应温度分别为
(2)直接电解吸收也是脱硝的一种方法。用6%的稀硝酸吸收NOx生成亚硝酸,再将吸收液导入电解槽电解,使之转化为硝酸。电解装置如右下图所示。阳极的电极反应式为

(Ⅱ)氨是重要的化工原料,工业合成氨有重要现实意义。
(1)在773K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中发生反应生成NH3,气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。

①下列能说明反应达到平衡状态的是
a.v正(N2)=3v逆(H2) b.体系压强不变
c.气体平均相对分子质量不变 d.气体密度不变
②在此温度下,若起始充入4.00mol N2和12.00mol H2,则反应刚达到平衡时,表示 c(H2)~t的曲线上相应的点为
(2)在373 K时,向体积为2L的恒容真空容器中充入0.40mol NO2,发生如下反应:2NO2(g)⇌N2O4(g) ∆H=-56.9kJ‧mol-1,测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
| t/min | 0 | 20 | 40 | 60 | 80 |
| φ(NO2) | 1.0 | 0.75 | 0.52 | 0.40 | 0.40 |
①计算0~20min时,v(N2O4)=
②已知该反应v正(NO2)=k1‧c2(NO2),v逆(N2O4)=k2‧c(N2O4),其中k1、k2为速率常数,则373K时,
19-20高三下·广东深圳·阶段练习
类题推荐
氮的化合物是重要的工业原料,也是主要的大气污染来源研究氮的化合物的反应具有重要意义。回答下列问题:
(1)肼(N2H4)与四氧化二氮分别是火箭发射器中最常用的燃料与氧化剂。已知3.2g液态肼与足量液态四氧化二氮完全反应,生成氮气和液态水放出热量61.25kJ,则该反应的热化学方程式为__ 。
(2)在773K时,分别将2.00molN2和6.00molH2充入一个固定容积为1L的密闭容器中发生反应生成NH3气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。
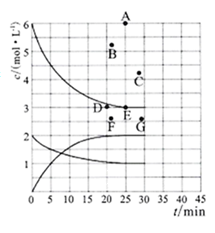
①下列能说明反应达到平衡状态的是__ 选填字母。
a.v正(N2)=v逆(H2)
b.体系压强不变
c.气体平均相对分子质量不变
d.气体密度不变
②在此温度下,若起始充入4.0molN2和12.0molH2,则反应刚达到平衡时,表示c(H2)~t的曲线上相应的点为__ (选填字母)。
(3)在373K时,向体积为2L的恒容真空容器中充入0.40molNO2发生如下反应:2NO2(g) N2O4(g)△H=-56.9kJ/mol。测得的NO2体积分数[φ(NO2)]与反应时间(t)的关系如表:
N2O4(g)△H=-56.9kJ/mol。测得的NO2体积分数[φ(NO2)]与反应时间(t)的关系如表:
①计算0~20min时,v(N2O4)=__ 。
②已知该反应v正(NO2)=k1·c2(NO2),v逆(N2O4)=k2·c(N2O4),其中k1、k2为速率常数,则373K时, =
=___ ;改变温度至T时,k1=k2,则T1__ 373K(填“>”、“<”或“=”)。
(1)肼(N2H4)与四氧化二氮分别是火箭发射器中最常用的燃料与氧化剂。已知3.2g液态肼与足量液态四氧化二氮完全反应,生成氮气和液态水放出热量61.25kJ,则该反应的热化学方程式为
(2)在773K时,分别将2.00molN2和6.00molH2充入一个固定容积为1L的密闭容器中发生反应生成NH3气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。

①下列能说明反应达到平衡状态的是
a.v正(N2)=v逆(H2)
b.体系压强不变
c.气体平均相对分子质量不变
d.气体密度不变
②在此温度下,若起始充入4.0molN2和12.0molH2,则反应刚达到平衡时,表示c(H2)~t的曲线上相应的点为
(3)在373K时,向体积为2L的恒容真空容器中充入0.40molNO2发生如下反应:2NO2(g)
| t/min | 0 | 20 | 40 | 60 | 80 |
| φ(NO2) | 1.0 | 0.75 | 0.52 | 0.40 | 0.40 |
②已知该反应v正(NO2)=k1·c2(NO2),v逆(N2O4)=k2·c(N2O4),其中k1、k2为速率常数,则373K时,
氮的化合物是重要的工业原料,也是主要的大气污染来源,研究氮的化合物的反应具有重要意义。回答下列问题:
(1)肼(N2H4)与四氧化二氮分别是火箭发射器中最常用的燃料与氧化剂。已知3.2g液态肼与足量液态四氧化二氮完全反应,生成氮气和液态水放出热量61. 25 kJ,则该反应的热化学方程式为____ 。
(2)尾气中的NO2可以用烧碱溶液吸收的方法来处理,其中能生成NaNO2等物质,该反应的离子方程式为____ 。
(3)在773 K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中发生反应生成NH3,气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。
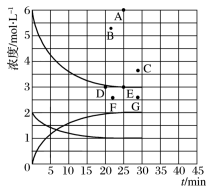
①下列能说明反应达到平衡状态的是____ (选填字母)。
a.v正(N2)=3v逆(H2) b.体系压强不变
c.气体平均相对分子质量不变 d.气体密度不变
②在此温度下,若起始充入4. 00 mol N2和12. 00 mol H2,则反应刚达到平衡时,表示 c(H2)~t的曲线上相应的点为___ (选填字母)。
(4)在373 K时,向体积为2L的恒容真空容器中充入0.40mol NO2,发生如下反应:
测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
①计算0~20min时,v(N2O4)=____ 。
②已知该反应 ,其中k1、k2为速率常数,则373K时,
,其中k1、k2为速率常数,则373K时, =
=_____ ;改变温度至T1时,k1=k2,则T1___ 373 K(填“>”“<”或“=”)。
(1)肼(N2H4)与四氧化二氮分别是火箭发射器中最常用的燃料与氧化剂。已知3.2g液态肼与足量液态四氧化二氮完全反应,生成氮气和液态水放出热量61. 25 kJ,则该反应的热化学方程式为
(2)尾气中的NO2可以用烧碱溶液吸收的方法来处理,其中能生成NaNO2等物质,该反应的离子方程式为
(3)在773 K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中发生反应生成NH3,气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。

①下列能说明反应达到平衡状态的是
a.v正(N2)=3v逆(H2) b.体系压强不变
c.气体平均相对分子质量不变 d.气体密度不变
②在此温度下,若起始充入4. 00 mol N2和12. 00 mol H2,则反应刚达到平衡时,表示 c(H2)~t的曲线上相应的点为
(4)在373 K时,向体积为2L的恒容真空容器中充入0.40mol NO2,发生如下反应:
测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
| t/min | 0 | 20 | 40 | 60 | 80 |
| φ(NO2) | 1.0 | 0.75 | 0.52 | 0.40 | 0.40 |
②已知该反应
消除氮氧化物和硫氧化物有多种方法。
(1)用活性炭还原法:某研究小组向某密闭容器中加入足量的活性炭和NO,发生反应:C(s)+2NO(g)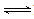 N2(g)+CO2(g) △H=Q kJ·mol-1在 T1℃下,反应进行到不同时间测得各物质的浓度部分数据如下:
N2(g)+CO2(g) △H=Q kJ·mol-1在 T1℃下,反应进行到不同时间测得各物质的浓度部分数据如下:
①0~10 min 内,N2的平均反应速率 υ(N2)=________ ,T1℃时,该反应的平衡常数 K=_____ 。
②30 min 后,若只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是____________ (填字母)
a. 加入一定量的活性炭 b. 改变反应体系的温度 c. 缩小容器的体积 d. 通入一定量的NO
③若30 min后升高温度至 T2℃,重新达到平衡时,容器中NO、N2、CO2的浓度之比为7∶3∶3,则该反应的△H______ 0(填“>” 、 “ =” 、或“<” )
(2)NH3催化还原法:原理如图所示
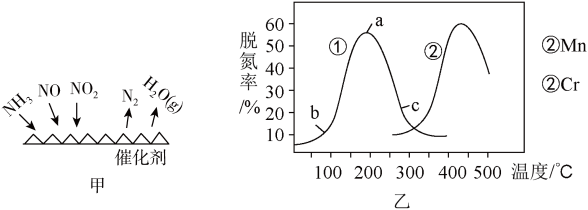
①若烟气中 c(NO2): c(NO)=1∶1,发生如图甲所示的脱氮反应时,反应过程中转移1.5mol电子时放出的热量为 113.8 kJ,则发生该脱氮反应的热化学方程式为_____ 。
②图乙是在一定时间内,使用不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应温度分别为___ ;使用Mn作催化剂时,脱氮率b~a段呈现如图变化的可能原因是___ 。
(3)直接电解吸收也是脱硝的一种方法。用6%的稀硝酸吸收NOx生成亚硝酸,再将吸收液导入电解槽电解,使之转化为硝酸。电解装置如图所示。
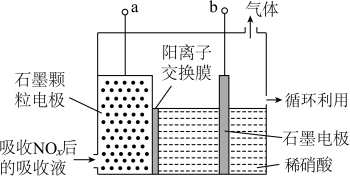
①图中b应连接电源的_________ (填“正极”或“负极”)。
②将石墨电极设置成颗粒状的目是_____________________ 。
③阳极的电极反应式为___________________ 。
(1)用活性炭还原法:某研究小组向某密闭容器中加入足量的活性炭和NO,发生反应:C(s)+2NO(g)
 N2(g)+CO2(g) △H=Q kJ·mol-1在 T1℃下,反应进行到不同时间测得各物质的浓度部分数据如下:
N2(g)+CO2(g) △H=Q kJ·mol-1在 T1℃下,反应进行到不同时间测得各物质的浓度部分数据如下:| 时间(min) 浓度mol/L | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.40 | 0.20 | 0.30 | 0.30 | |
| N2 | 0 | 0.40 | 0.60 | 0.60 | ||
| CO2 | 0 | 0.60 | 0.60 |
①0~10 min 内,N2的平均反应速率 υ(N2)=
②30 min 后,若只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是
a. 加入一定量的活性炭 b. 改变反应体系的温度 c. 缩小容器的体积 d. 通入一定量的NO
③若30 min后升高温度至 T2℃,重新达到平衡时,容器中NO、N2、CO2的浓度之比为7∶3∶3,则该反应的△H
(2)NH3催化还原法:原理如图所示

①若烟气中 c(NO2): c(NO)=1∶1,发生如图甲所示的脱氮反应时,反应过程中转移1.5mol电子时放出的热量为 113.8 kJ,则发生该脱氮反应的热化学方程式为
②图乙是在一定时间内,使用不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应温度分别为
(3)直接电解吸收也是脱硝的一种方法。用6%的稀硝酸吸收NOx生成亚硝酸,再将吸收液导入电解槽电解,使之转化为硝酸。电解装置如图所示。

①图中b应连接电源的
②将石墨电极设置成颗粒状的目是
③阳极的电极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


