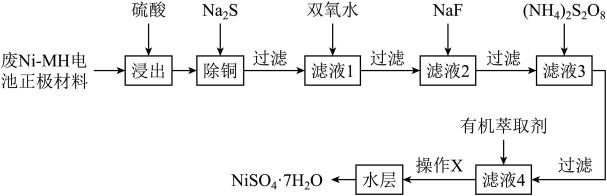
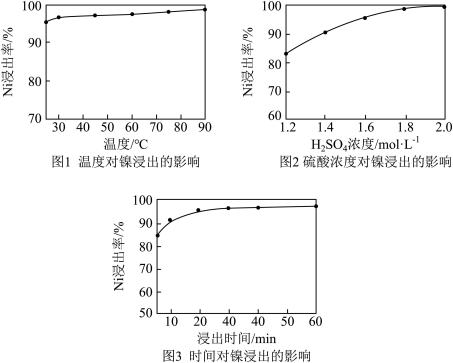
解答题-工业流程题 适中0.65 引用1 组卷154
2020年5月5日晚18时00分,我国载人空间站货物返回舱试验舱在我国文昌航天发射场点火升空,5月8日飞船试验船返回舱在东风着陆场预定区域成功着陆,试验取得圆满成功。金属铍(Be)是火箭、航空、宇宙航行的重要材料,工业上以含铍废渣(主要成分是Be和MgF2)为原料制备金属铍的工艺流程。如图:
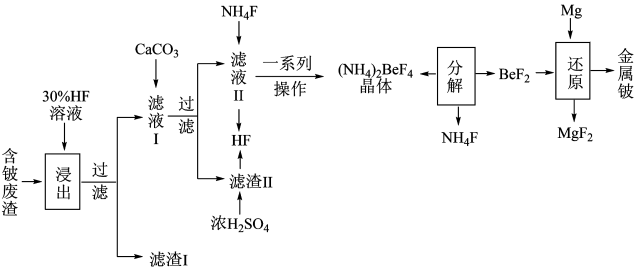
已知:MgF2和CaF2难溶于水。回答下列问题:
(1)提高浸出速率的方法有___ 、__ (任写两项);已知滤液Ⅰ中铍元素的存在形式为H2BeF4,写出“浸出”过程中发生反应的化学方程式:__ 。
(2)该流程中可循环利用的物质是__ ;滤渣Ⅱ与浓硫酸发生反应的化学方程式为___ ;已知(NH4)2BeF4易溶于水,且其在水中的溶解度随温度的升高而大幅度增大,从NH4F与滤液Ⅱ发生反应后所得溶液中获得(NH4)2BeF4晶体的“一系列操作”具体是指__ 过滤、洗涤、干燥。
(3)“分解”过程中产生的BeF2在熔融状态下不能导电,其电子式为___ ;“还原”过程可以用金属镁制备金属铍的原因是__ 。

已知:MgF2和CaF2难溶于水。回答下列问题:
(1)提高浸出速率的方法有
(2)该流程中可循环利用的物质是
(3)“分解”过程中产生的BeF2在熔融状态下不能导电,其电子式为
19-20高三下·江西上饶·阶段练习
类题推荐
铍是一种重要金属,主要用于原子能反应堆材料,宇航工程材料。根据元素周期表的对角线规则可知Be和Al性质相似,工业上常用绿柱石(主要成分为3BeO·Al2O3·6SiO2,还含有铁等杂质)冶炼铍,工艺流程如图所示:
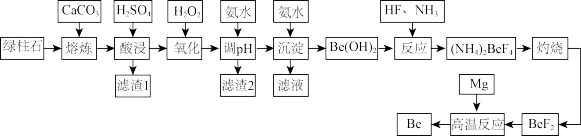
已知:几种物质沉淀时的pH如下表:
回答下列问题:
(1)“酸浸”时为提高效率可以采取的措施是_______ 。(任写两条)。滤渣1的主要成分为_______ (写化学式)。
(2)“氧化”的目的是_______ 。
(3)“调pH”产生沉淀,其合理pH范围是_______ 。
(4)“沉淀”反应不宜使用NaOH溶液的原因是(用离子方程式表示)_______ 。
(5)从“反应”后的溶液中得到(NH4)2BeF4固体的实验操作是_______ 、_______ 、过滤、洗涤、干燥。
(6)“高温反应”需要在隔绝空气的环境中进行,其原因是_______ 。

已知:几种物质沉淀时的pH如下表:
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Be(OH)2 | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 5.2 |
| 沉淀完全时 | 3.7 | 5.0 | 9.7 | 8.8 |
(1)“酸浸”时为提高效率可以采取的措施是
(2)“氧化”的目的是
(3)“调pH”产生沉淀,其合理pH范围是
(4)“沉淀”反应不宜使用NaOH溶液的原因是(用离子方程式表示)
(5)从“反应”后的溶液中得到(NH4)2BeF4固体的实验操作是
(6)“高温反应”需要在隔绝空气的环境中进行,其原因是
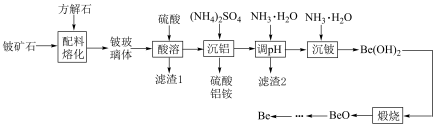
Be是重要的战略性金属,其性质与铝相似。以铍矿石、方解石为原料制备铍的工艺流程如图所示: (氧化物形式为
(氧化物形式为 ),还含有Fe2O3(忽略其他元素对工艺流程的影响);方解石的主要成分为CaCO3;铍玻璃体的主要成分为CaAl2Si2O8、CaBe3SiO6,Fe2O3、SiO2;
),还含有Fe2O3(忽略其他元素对工艺流程的影响);方解石的主要成分为CaCO3;铍玻璃体的主要成分为CaAl2Si2O8、CaBe3SiO6,Fe2O3、SiO2;
②硫酸铝铵微溶于水;常温下,相关物质溶度积如下表所示:
回答下列问题:
(1)提高“配料熔化”时的反应速率及效率的措施为___________ (任写一条),该过程中主要反应的化学方程式为___________ 。
(2)“酸溶”时CaBe3SiO6发生反应的离子方程式为___________ 。
(3)常温下,“调pH”时所得滤液的pH为5,则“滤渣2”的成分为___________ (填化学式,下同)。该工业流程中可循环使用的物质为___________ 。
(4)常温时调节pH为7.5进行“沉铍”,通过计算判断 是否完全沉淀:
是否完全沉淀:___________ (溶液中离子浓度低于 时认为该离子完全沉淀);“沉铍”时不选用NaOH溶液的原因为
时认为该离子完全沉淀);“沉铍”时不选用NaOH溶液的原因为___________ (用离子方程式解释)。
(5)先将原料BeO与碳质还原剂压制成团块,再在高温下将其氯化为BeCl2,然后用镍坩埚为阴极,石墨棒为阳极,将等量的BeCl2与氯化钠混合熔融后进行电解,在___________ (填“阴”或“阳”)极上析出固态金属铍,该法的缺点为___________ 。
②硫酸铝铵微溶于水;常温下,相关物质溶度积如下表所示:
| 难溶物 | |||
(1)提高“配料熔化”时的反应速率及效率的措施为
(2)“酸溶”时CaBe3SiO6发生反应的离子方程式为
(3)常温下,“调pH”时所得滤液的pH为5,则“滤渣2”的成分为
(4)常温时调节pH为7.5进行“沉铍”,通过计算判断
(5)先将原料BeO与碳质还原剂压制成团块,再在高温下将其氯化为BeCl2,然后用镍坩埚为阴极,石墨棒为阳极,将等量的BeCl2与氯化钠混合熔融后进行电解,在
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网