解答题-实验探究题 适中0.65 引用1 组卷119
一水硫酸四氨合铜晶体[Cu(NH3)4SO4·H2O,相对分子质量为246]是一种重要的染料及农药中间体。常温下该物质可溶于水,难溶于乙醇。某化学兴趣小组通过以下实验制备一水硫酸四氨合铜晶体并测定其纯度。回答相关问题:
I.实验室制取CuSO4溶液
方案i:铜与浓硫酸加热制备。
方案ii:将铜粉在空气中充分加热至完全变黑,再加稀硫酸即可得到硫酸铜溶液。
(1)请写出方案i反应的化学方程式________________________________________ ,此方法硫酸的利用率较低的原因是___________________________ (写1点)。
(2)实际生产中方案ii常常有紫红色固体未反应,猜想原因可能是___________ 。
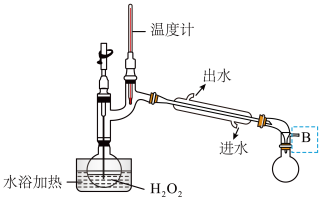
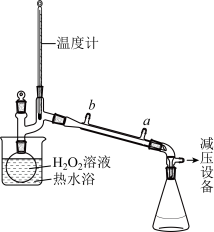
(3)某同学对实验ii进行了改进,其中一种方案是在硫酸和铜的反应容器中滴加H2O2溶液,观察到的现象是_____________________________________ 。H2O2的沸点为150.2℃。为加快反应需要提高H2O2溶液的浓度,可通过如图将H2O2稀溶液浓缩,增加减压设备的目的除了加快蒸馏速度,还有可能是________________________ 。
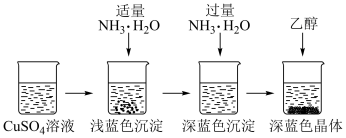
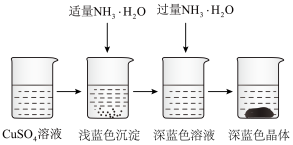
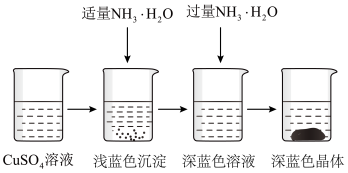
II.一水硫酸四氨合铜晶体的制备
(4)硫酸铜溶液含有一定的硫酸,呈酸性,加入适量NH3·H2O调节溶液pH,产生浅蓝色沉淀,已知其成分为Cu2(OH)2SO4,试写出生成此沉淀的离子反应方程式_______________________ 。
(5)继续滴加NH3·H2O,会转化成深蓝色溶液。向深蓝色溶液中加入乙醇可析出深蓝色晶体,滴加乙醇的作用可能是________________
A.乙醇可以作还原剂
B.乙醇可以降低该晶体在该溶液中的溶解度
C.乙醇可以作萃取剂
Ⅲ.产品纯度的测定
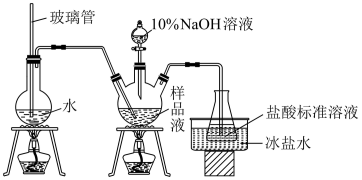
(6)精确称取mg晶体,加适量水溶解,然后逐滴加入足量NaOH溶液,通入水蒸气将氨全部蒸出,用V1mL0.200mol·L-1的盐酸完全吸收。以甲基橙作指示剂,用0.200mol·L-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。产品纯度的表达式为____________ 。
I.实验室制取CuSO4溶液
方案i:铜与浓硫酸加热制备。
方案ii:将铜粉在空气中充分加热至完全变黑,再加稀硫酸即可得到硫酸铜溶液。
(1)请写出方案i反应的化学方程式
(2)实际生产中方案ii常常有紫红色固体未反应,猜想原因可能是
(3)某同学对实验ii进行了改进,其中一种方案是在硫酸和铜的反应容器中滴加H2O2溶液,观察到的现象是

II.一水硫酸四氨合铜晶体的制备
(4)硫酸铜溶液含有一定的硫酸,呈酸性,加入适量NH3·H2O调节溶液pH,产生浅蓝色沉淀,已知其成分为Cu2(OH)2SO4,试写出生成此沉淀的离子反应方程式
(5)继续滴加NH3·H2O,会转化成深蓝色溶液。向深蓝色溶液中加入乙醇可析出深蓝色晶体,滴加乙醇的作用可能是
A.乙醇可以作还原剂
B.乙醇可以降低该晶体在该溶液中的溶解度
C.乙醇可以作萃取剂
Ⅲ.产品纯度的测定
(6)精确称取mg晶体,加适量水溶解,然后逐滴加入足量NaOH溶液,通入水蒸气将氨全部蒸出,用V1mL0.200mol·L-1的盐酸完全吸收。以甲基橙作指示剂,用0.200mol·L-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。产品纯度的表达式为
19-20高三·宁夏银川·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网