填空题 适中0.65 引用1 组卷118
铁及其化合物用途非常广泛。
(1)已知赤铁矿还原冶炼时是逐级进行的,已知:
(a) 3Fe2O3(s)+CO(g) 2Fe3O4(s)+CO2(g)
2Fe3O4(s)+CO2(g)  H = a kJ·mol-1
H = a kJ·mol-1
(b) Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)  H =b kJ·mol-1
H =b kJ·mol-1
(c) Fe3O4(s)+CO(g) 3FeO(s)+CO2 (g)
3FeO(s)+CO2 (g)  H = c kJ·mol-1
H = c kJ·mol-1
①上述反应(a)平衡常数表达式为K=___________________ 。
②反应FeO(s)+CO(g) Fe(s)+CO2(g)
Fe(s)+CO2(g)  H =
H =__________ kJ·mol-1(用含a、b、c的代数式表示)。
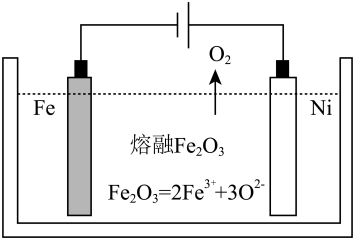
(2)用类似冶炼铝的方法, 在600~1000℃时电解熔融的Fe2O3冶炼铁(装置示意图如图),该法除消耗能量较少外,另一最突出的优点是__________________________________ ;电解时阳极发生的电极反应为____________ 。
(3)生铁在自然界中可发生析氢腐蚀和吸氧腐蚀,析氢腐蚀的负极的电极反应式为_________ ;如图所示,纯铁处于a、b、c三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填字母)_____________ 。

(1)已知赤铁矿还原冶炼时是逐级进行的,已知:
(a) 3Fe2O3(s)+CO(g)
(b) Fe2O3(s)+3CO(g)
(c) Fe3O4(s)+CO(g)
①上述反应(a)平衡常数表达式为K=
②反应FeO(s)+CO(g)
(2)用类似冶炼铝的方法, 在600~1000℃时电解熔融的Fe2O3冶炼铁(装置示意图如图),该法除消耗能量较少外,另一最突出的优点是

(3)生铁在自然界中可发生析氢腐蚀和吸氧腐蚀,析氢腐蚀的负极的电极反应式为

19-20高二下·江苏盐城·期中
类题推荐
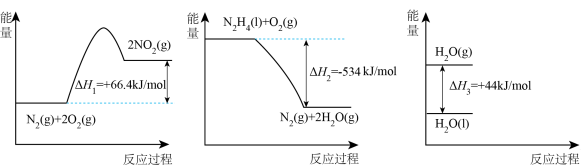
化学反应中均伴随有能量变化。
(1)下列反应中,反应物的总能量小于生成物的总能量的为____ (填选项字母)。
(2)已知25℃时,相关物质的相对能量如表所示;
①表示H2(g)燃烧热的热化学方程为____ 。
②0.5molH2O(g)转化为H2O(l)需要____ (填“吸收”或“放出”)____ kJ的热量。
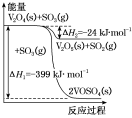
(3)已知:
Ⅰ.2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1
Ⅱ.C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1
根据盖斯定律计算CO(g)+ O2(g)=CO2(g) △H=
O2(g)=CO2(g) △H=____ kJ·mol-1。
(1)下列反应中,反应物的总能量小于生成物的总能量的为
| A.Na与水反应 | B.甲烷的燃烧反应 | C.CaCO3受热分解 | D.锌与盐酸反应 |
| 物质 | H2(g) | O2(g) | H2O(g) | H2O(l) |
| 相对能量(kJ·mol-1) | 0 | 0 | -242 | -286 |
①表示H2(g)燃烧热的热化学方程为
②0.5molH2O(g)转化为H2O(l)需要
(3)已知:
Ⅰ.2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1
Ⅱ.C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1
根据盖斯定律计算CO(g)+
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网