解答题-原理综合题 适中0.65 引用3 组卷463
碳及其化合物在工农业生产和日常生活中有广泛的应用,对其研究具有重要意义。
回答下列问题:
(1)利用活性炭的___ 作用可去除水中的悬浮杂质。
(2)炭黑可以活化氧分子得到活化氧(O*),活化氧可以快速将SO2氧化为SO3,其活化过程中的能量变化如图所示:
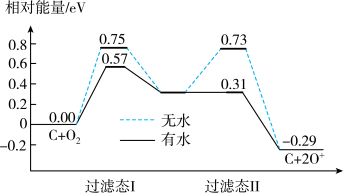
活化过程中有水时的活化能降低了___ eV。在酸雨的形成过程中,炭黑起:___ 作用。
(3)已知:CO(g)+2H2(g) CH3OH(g) ∆H,经测定不同温度下该反应的浓度平衡常数如下:
CH3OH(g) ∆H,经测定不同温度下该反应的浓度平衡常数如下:
①该反应的△H___ 0(填“>”或“<");250℃时,某时刻测得反应体系中c(CO)=0.4mol·L-1、c(H2)=0.4mol·L-1、c(CH3OH)=0.8mol·L-1,则此时v正__ v逆(填“>”、“=”或“<”)。.
②某温度下,在2L刚性容器中,充入0.8molCO和1.6molH2,压强为p,tmin后达到平衡,测得压强为 P。则v(H2)=
P。则v(H2)=____ mol·L-1·min-1,平衡时的Kp=____ 。
(4)科研人员设计了甲烷燃料电池电解饱和食盐水装置如图所示,电池的电解质是掺杂了Y2O3与ZrO2的固体,可在高温下传导O2-。
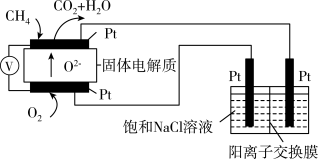
①该电池工作时负极反应方程式为____ 。
②用该电池电解100mL饱和食盐水,若在两极产生的气体体积分别为V1L、V2L(标准状况),且V1>V2,则电解所得溶液的c(OH-)=____ mol·L-1(忽略气体溶解和溶液体积变化)。
回答下列问题:
(1)利用活性炭的
(2)炭黑可以活化氧分子得到活化氧(O*),活化氧可以快速将SO2氧化为SO3,其活化过程中的能量变化如图所示:

活化过程中有水时的活化能降低了
(3)已知:CO(g)+2H2(g)
| 温度/℃ | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,在2L刚性容器中,充入0.8molCO和1.6molH2,压强为p,tmin后达到平衡,测得压强为
(4)科研人员设计了甲烷燃料电池电解饱和食盐水装置如图所示,电池的电解质是掺杂了Y2O3与ZrO2的固体,可在高温下传导O2-。

①该电池工作时负极反应方程式为
②用该电池电解100mL饱和食盐水,若在两极产生的气体体积分别为V1L、V2L(标准状况),且V1>V2,则电解所得溶液的c(OH-)=
2020·湖北武汉·模拟预测
类题推荐
甲烷是一种重要的化工原料,广泛应用于工业中。回答下列问题:
(1)甲烷在工业上可用于制备合成气: ,在某密闭容器中通入
,在某密闭容器中通入 和
和 ,在不同条件下发生反应。测得平衡时
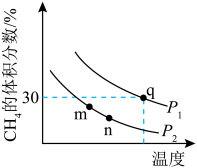
,在不同条件下发生反应。测得平衡时 的体积分数与温度、压强的关系如图所示。
的体积分数与温度、压强的关系如图所示。
___________ (填“<”、“>”或“=”下同)P2,
___________ 0。
② 三点的化学平衡常数大小关系为
三点的化学平衡常数大小关系为___________ 。
③ 点甲烷的转化率为
点甲烷的转化率为___________ 。
(2)甲烷在一定条件下脱氢可生成乙烯,其反应如下: 。
。 温度下,在体积为
温度下,在体积为 的刚性密闭容器中充入
的刚性密闭容器中充入 甲烷进行上述反应,容器内的总压强
甲烷进行上述反应,容器内的总压强 随时间
随时间 的变化如下表所示:
的变化如下表所示:
①下列有关说法正确的是___________ 。
A.当混合气的密度不变时,表明该反应已达到平衡状态
B.反应进行到第10分钟时刚好达到平衡
C.升温既可提高反应速率也能提高甲烷的转化率
D.使用适当的催化剂既可提高反应速率也能提高甲烷的转化率
E.该反应在较高温度下可自发进行
②前10min内,平均速率v(H2)=___________ kPa·min-1,实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2),其中k正、k逆为速率常数,仅与温度有关,T1温度时,k正/k逆=___________ (填数值)。
(3)科研人员设计了甲烷燃料电池电解饱和食盐水装置如图所示,电池的电解质是掺杂了Y2O3与ZrO2的固体,可在高温下传导O2-。___________ 。
②用该电池电解100mL饱和食盐水,若电解一段时间后,两极产生的气体体积分别为0.224L和0.336L(均为标准状况),则电解所得溶液的pH=___________ (忽略气体溶解和溶液体积变化)。
(1)甲烷在工业上可用于制备合成气:
②
③
(2)甲烷在一定条件下脱氢可生成乙烯,其反应如下:
| 反应时间/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
| 总压强P/kPa | 10.0 | 11.5 | 12.3 | 13.0 | 13.6 | 14.0 | 14.0 |
A.当混合气的密度不变时,表明该反应已达到平衡状态
B.反应进行到第10分钟时刚好达到平衡
C.升温既可提高反应速率也能提高甲烷的转化率
D.使用适当的催化剂既可提高反应速率也能提高甲烷的转化率
E.该反应在较高温度下可自发进行
②前10min内,平均速率v(H2)=
(3)科研人员设计了甲烷燃料电池电解饱和食盐水装置如图所示,电池的电解质是掺杂了Y2O3与ZrO2的固体,可在高温下传导O2-。
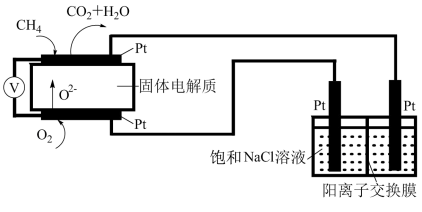
②用该电池电解100mL饱和食盐水,若电解一段时间后,两极产生的气体体积分别为0.224L和0.336L(均为标准状况),则电解所得溶液的pH=
碳单质及其化合物在生产生活中用途广泛。
I.单质碳经常应用于化学反应中。回答以下问题:_______ 0 (填‘‘>”、“<”或“=”),活化过程中有水时的活化能降低了_______ eV。
(2)以焦炭为原料,在高温下与水蒸气反应可制得水煤气,涉及反应如下:
a.C(s)+H2O(g)=CO(g)+H2(g) ∆H1
b.C(s)+2H2O(g)=CO2(g)+2H2(g) ∆H2=+90.3kJ·mol-1
c.CO(g)+H2O(g)=CO2(g)+H2(g) ∆H3=-41.0kJ·mol-1
①∆H1=_______ kJ·mol-1。
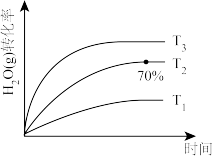
②对于反应a,测得在不同温度下H2O(g)的转化率如图所示,图中T1、T2、T3的大小关系为_______ 。用物质的平衡分压代替物质的量浓度也可以表示化学反应的平衡常数(Kp),在T2℃、50 MPa时,反应a的平衡常数Kp=_______ MPa(已知气体分压=气体总压×各气体的体积分数,列出计算式并代入数据,无需化简)。
(3)CO2对甲醇合成的影响是_______ 。
Ⅲ.锂硒电池具有优异的循环稳定性。
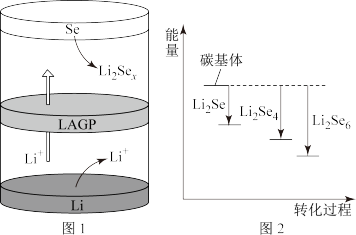
(4)一种锂硒电池放电时的工作原理如图l所示,正极的电极反应式为_______ 。Li2Sex与正极碳基体结合时的能量变化如图2所示,图中3种Li2Sex与碳基体的结合能力的大小顺序是_______ 。
I.单质碳经常应用于化学反应中。回答以下问题:
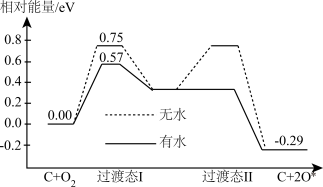
(2)以焦炭为原料,在高温下与水蒸气反应可制得水煤气,涉及反应如下:
a.C(s)+H2O(g)=CO(g)+H2(g) ∆H1
b.C(s)+2H2O(g)=CO2(g)+2H2(g) ∆H2=+90.3kJ·mol-1
c.CO(g)+H2O(g)=CO2(g)+H2(g) ∆H3=-41.0kJ·mol-1
①∆H1=
②对于反应a,测得在不同温度下H2O(g)的转化率如图所示,图中T1、T2、T3的大小关系为
| CO2%-CO%-H2% (体积分数) | 0-30-70 | 4-26-70 | 8-22-70 | 20-10-70 | |||||||||
| 反应温度/℃ | 225 | 235 | 250 | 225 | 235 | 250 | 225 | 235 | 250 | 225 | 235 | 250 | |
| 碳转化 | CH3OH | 4.9 | 8.8 | 11.0 | 19.0 | 33.1 | 56.5 | 17.7 | 33.4 | 54.4 | 8.0 | 12.0 | 22.6 |
| 率(%) | CH4 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 2.8 | 2.8 | 2.8 |
Ⅲ.锂硒电池具有优异的循环稳定性。
(4)一种锂硒电池放电时的工作原理如图l所示,正极的电极反应式为
甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g) CH3OH(g) ΔH1=-90 kJ·mol-1
CH3OH(g) ΔH1=-90 kJ·mol-1
②CO(g)+H2O(g)== CO2(g) +H2(g) ΔH2=-41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式______________ ;
(2)在一定条件下,某密闭容器中进行上述二氧化碳与氢气制备甲醇的反应,反应过程中部分数据如下表:
①0〜l0min内,用H2O(g)表示的化学反应速率v(H2O)=__ mol/(L·s)
②达到平衡时,该反应的平衡常数K=____ (用分数表示),平衡时H2的转化率是____ 。
③在其它条件不变的情况下,若30min时改变温度为T2℃,此时H2的物质的量为3.2mol,则T1___ T2(填“>”、“<”或“=”),理由是_____ 。在其他条件不变的情况下,若30min时向容器中再充入lmolCO2(g)和lmolH2O (g),则平衡____ 移动(填“正向”、“逆向”或“不”)。
(3)以甲醇为燃料的新型燃料电池,正极通入O2,负极通入甲醇,在酸性溶液中甲醇与氧作用生成水和二氧化碳。
①负极的电极反应式是________________ ;
②若以该燃料电池作为电源,用石墨作电极电解500mL饱和食盐水,当两极共收集到标准状况下的气体1.12L (不考虑气体的溶解)时,所得溶液的pH=____ (假设反应前后溶液体积不变)。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g)
 CH3OH(g) ΔH1=-90 kJ·mol-1
CH3OH(g) ΔH1=-90 kJ·mol-1②CO(g)+H2O(g)== CO2(g) +H2(g) ΔH2=-41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式
(2)在一定条件下,某密闭容器中进行上述二氧化碳与氢气制备甲醇的反应,反应过程中部分数据如下表:
| 反应条件 | 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
| 恒温恒容 (T1℃、2L) | Omin | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 |
①0〜l0min内,用H2O(g)表示的化学反应速率v(H2O)=
②达到平衡时,该反应的平衡常数K=
③在其它条件不变的情况下,若30min时改变温度为T2℃,此时H2的物质的量为3.2mol,则T1
(3)以甲醇为燃料的新型燃料电池,正极通入O2,负极通入甲醇,在酸性溶液中甲醇与氧作用生成水和二氧化碳。
①负极的电极反应式是
②若以该燃料电池作为电源,用石墨作电极电解500mL饱和食盐水,当两极共收集到标准状况下的气体1.12L (不考虑气体的溶解)时,所得溶液的pH=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


