解答题-原理综合题 适中0.65 引用1 组卷28
CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为______ (写离子符号);若所得溶液c( )∶c(
)∶c( )=2∶1,溶液pH=
)=2∶1,溶液pH=___________ 。(室温下,H2CO3的K1=4×10−7;K2=5×10−11)
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+ CO2(g) 2CO (g)+ 2H2(g),已知上述反应中相关的化学键键能数据如下:
2CO (g)+ 2H2(g),已知上述反应中相关的化学键键能数据如下:
则该反应的ΔH=_________ 。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是_______ (填“A” 或“B ”)。
(3)O2辅助的Al~CO2电池工作原理如图所示。
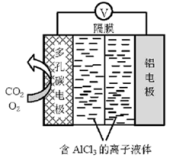
该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。电池的负极反应式:________ ,电池的正极反应式:6O2+6e−=6O ;6CO2+6O2−=3
;6CO2+6O2−=3 + 6O2,反应过程中O2的作用是
+ 6O2,反应过程中O2的作用是________ 。
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+ CO2(g)
| 化学键 | C—H | C=O | H—H | C |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=
(3)O2辅助的Al~CO2电池工作原理如图所示。

该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。电池的负极反应式:
18-19高二上·江西九江·阶段练习
类题推荐
CO2是一种廉价的碳资源,其综合利用具有重要意义,回答下列问题:
(1) CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g) 2CO(g)+2H2(g)。
2CO(g)+2H2(g)。
①已知上述反应中相关的化学键键能数据如下:
则该反应的ΔH=_______ 。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是________ (填“A”或“B”)。
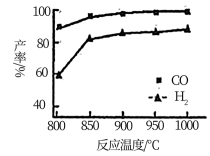
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图所示。此反应优选温度为900℃的原因是_______ 。
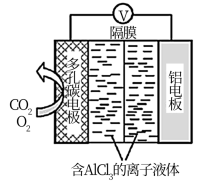
(2) O2辅助的Al-CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料,电池的正极反应式:6O2+6e-=6O 、
、 ,反应过程中O2的作用是
,反应过程中O2的作用是________ ,该电池的总反应化学方程式是_____________ 。
(3)汽车尾气净化装置中,发生反应:2NO(g)+2CO(g)⇌N2(g)+2CO2(g)△H2=-746.8 kJ•mol-1,已知v 正=k 正•c2(NO)•c2(CO),v 逆=k 逆•c(N2)•c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数________ (填“>”“<”或“=”) k逆增大的倍数。
②若在1L的密闭容器中充入1 molCO和1 molNO,在一定温度下达到平衡时,CO的转化率为40%,则
_______ (保留2位有效数字)。
(4)已知钼酸钠(Na2MoO4)溶液中c( )=0.40mol•L-1,c(
)=0.40mol•L-1,c( )=0.52mol•L-1,由钼酸钠溶液制备钼酸钠晶体时,需加入Ba(OH)2固体以除去
)=0.52mol•L-1,由钼酸钠溶液制备钼酸钠晶体时,需加入Ba(OH)2固体以除去 ,当BaMoO4开始沉淀时,
,当BaMoO4开始沉淀时, 的去除率为
的去除率为_______ .[已知:Ksp(BaMoO4)=4.0×10-8,Ksp(BaCO3)=2.6×10-9,忽略溶液的体积变化]
(1) CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)
①已知上述反应中相关的化学键键能数据如下:
化学键 | ||||
键能/kJ·mol-1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图所示。此反应优选温度为900℃的原因是

(2) O2辅助的Al-CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料,电池的正极反应式:6O2+6e-=6O

(3)汽车尾气净化装置中,发生反应:2NO(g)+2CO(g)⇌N2(g)+2CO2(g)△H2=-746.8 kJ•mol-1,已知v 正=k 正•c2(NO)•c2(CO),v 逆=k 逆•c(N2)•c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数
②若在1L的密闭容器中充入1 molCO和1 molNO,在一定温度下达到平衡时,CO的转化率为40%,则
(4)已知钼酸钠(Na2MoO4)溶液中c(
CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
I.CO2可以被NaOH溶液捕获,若所得溶液c(HCO3-)∶c(CO32-)=2∶1,溶液pH=___ 。(室温下,H2CO3的K1=4×10-7;K2=5×10-11)
II.CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g) 2CO(g)+2H2(g)
2CO(g)+2H2(g)
(1)已知上述反应中相关的化学键键能数据:
则该反应的ΔH=___________ 。分别在V L恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是___________ (填“A”或“B”)。
(2)按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图1所示。此反应优选温度为900℃的原因是____________ 。
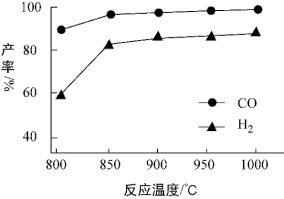
(3)在T1温度时,将CH4和CO2各1.0 mol充入2 L密闭恒容容器中,充分反应达到平衡后,若CH4转化率为40%,则
①容器内的压强与起始压强之比为___________ ;
②此温度下,若该容器中含有CH4、CO2、H2、CO各1.0 mol,则此时反应所处的状态为___________ (填“向正反应方向进行中”“向逆反应方向进行中”或“平衡状态”)
③欲使甲烷的平衡转化率提高,应采取的措施是___________ (填标号)。
A.升高温度 B.降低温度 C.增大压强 D.减小压强
I.CO2可以被NaOH溶液捕获,若所得溶液c(HCO3-)∶c(CO32-)=2∶1,溶液pH=
II.CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)
(1)已知上述反应中相关的化学键键能数据:
| 化学键 | C-H | C=O | H-H | 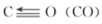 |
| 键能/kJ/mol | 413 | 745 | 436 | 1075 |
则该反应的ΔH=
(2)按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图1所示。此反应优选温度为900℃的原因是

(3)在T1温度时,将CH4和CO2各1.0 mol充入2 L密闭恒容容器中,充分反应达到平衡后,若CH4转化率为40%,则
①容器内的压强与起始压强之比为
②此温度下,若该容器中含有CH4、CO2、H2、CO各1.0 mol,则此时反应所处的状态为
③欲使甲烷的平衡转化率提高,应采取的措施是
A.升高温度 B.降低温度 C.增大压强 D.减小压强
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网