解答题-工业流程题 适中0.65 引用1 组卷217
马日夫盐 用于钢铁制品,特别是大型机械设备的磷化处理,可起到防锈效果。以软锰矿(主要成分为
用于钢铁制品,特别是大型机械设备的磷化处理,可起到防锈效果。以软锰矿(主要成分为 及少量的FeO、
及少量的FeO、 和
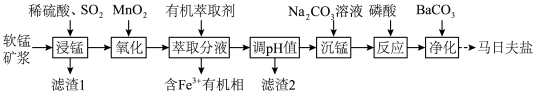
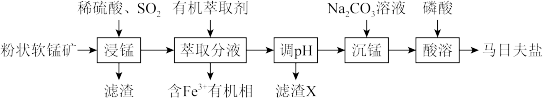
和 )为原料制备马日夫盐的主要工艺流程如图:
)为原料制备马日夫盐的主要工艺流程如图:
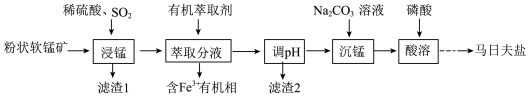
(1)“浸锰”过程中,FeO参与氧化还原反应的离子方程式为_______________ 。
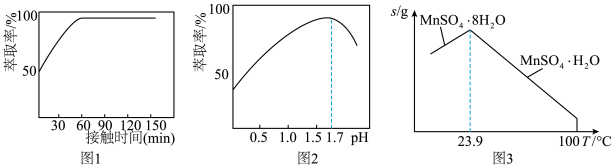
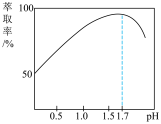
(2) 的萃取率与溶液的pH的关系如图所示,当
的萃取率与溶液的pH的关系如图所示,当 时,
时, 的萃取率急剧下降的原因可能为
的萃取率急剧下降的原因可能为_______________ (用化学用语表示)。
(3)“调pH”的最大范围为________ 。
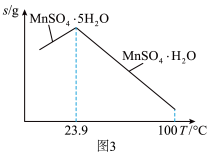
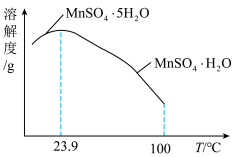
(4)如图为硫酸锰水合物的溶解度曲线,若要用“调pH”所得滤液制备 ,需要控制温度在80℃~90℃之间的原因是
,需要控制温度在80℃~90℃之间的原因是_____ ,采用水浴加热,经蒸发浓缩、_____ (填操作名称)、用80℃~90℃的蒸馏水洗涤2~3次,放在真空干燥箱中低温干燥获得。
(5)写出检验“沉锰”是否已完成的实验操作_________ 。
(6)常温下,马日夫盐溶液显________ 性(填“酸”或“碱”),理由是:____________ 。(写出计算过程并结合必要的文字说明。已知: 的电离常数
的电离常数 ,
, ,
, )
)

(1)“浸锰”过程中,FeO参与氧化还原反应的离子方程式为
(2)

(3)“调pH”的最大范围为
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| l. 8 | 3.2 | |
| 3.0 | 5.0 | |
| 5.8 | 8.8 | |
| 7.8 | 9.8 |
(4)如图为硫酸锰水合物的溶解度曲线,若要用“调pH”所得滤液制备

(5)写出检验“沉锰”是否已完成的实验操作
(6)常温下,马日夫盐溶液显
2020·福建漳州·三模
类题推荐
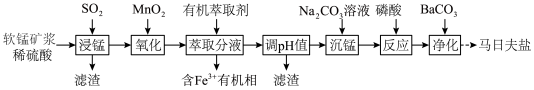
马日夫盐[Mn(H2PO4)2·2H2O]可用于钢铁的磷化处理,起到防锈作用。以软锰矿(主要成分为MnO2,少量FeO、Al2O3和SiO2)为原料制备马日夫盐的主要工艺流程如图:
已知:各金属离子开始沉淀和完全沉淀的pH如下表。
(1)“浸锰”时,SO2发生反应的离子方程式为___________ 。
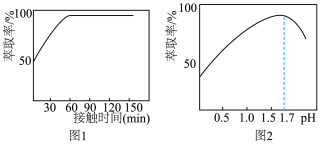
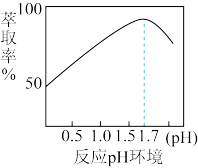
(2)“萃取”时,Fe3+的萃取率与溶液的pH的关系如下图所示,当pH>1.7时,Fe3+的萃取率急剧下降的原因可能为___________ 。
(3)“调pH”时,应调整的pH范围为___________ 。
(4)“沉锰”时,需将Na2CO3溶液逐渐加入锰盐溶液中,不能颠倒滴加顺序的原因是___________ 。检验“沉锰”是否已完成的实验操作是___________ 。
(5)“酸溶”时,生成马日夫盐的化学反应方程式为___________ 。

已知:各金属离子开始沉淀和完全沉淀的pH如下表。
| 金属离子 | Fe3+ | Al3+ | Fe2+ | Mn2+ |
| 开始沉淀的pH | 1.1 | 3.7 | 5.8 | 7.8 |
| 完全沉淀的pH | 3.0 | 5.0 | 8.8 | 9.8 |
(1)“浸锰”时,SO2发生反应的离子方程式为
(2)“萃取”时,Fe3+的萃取率与溶液的pH的关系如下图所示,当pH>1.7时,Fe3+的萃取率急剧下降的原因可能为

(3)“调pH”时,应调整的pH范围为
(4)“沉锰”时,需将Na2CO3溶液逐渐加入锰盐溶液中,不能颠倒滴加顺序的原因是
(5)“酸溶”时,生成马日夫盐的化学反应方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网