单选题 适中0.65 引用3 组卷294
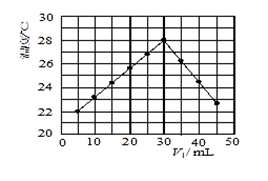
在 25 mL 1.00 mol/L HCl 溶液中逐滴加入未知浓度 NaOH 溶液 V mL,将溶液搅拌均匀后,在保温隔热的条件下测量并记录混合溶液的温度,实验结果如图所示。下列叙述正确的是

| A.做该实验时环境温度为22℃ |
| B.加入30 mLNaOH 溶液时,HCl完全被中和 |
| C.NaOH 溶液的物质的量浓度约为1.0 mol/L |
| D.该实验表明热能可能转化为化学能 |
19-20高一下·陕西西安·阶段练习
类题推荐
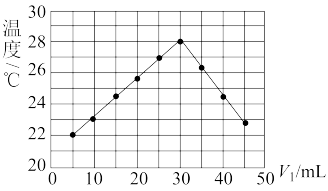
将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50)。下列叙述正确的是

| A.做该实验时环境温度小于22 ℃ |
| B.该实验表明化学能可以转化为热能 |
| C.NaOH溶液的浓度约是1.0 mol/L |
| D.该实验表明有水生成的反应都是放热反应 |
回答下列问题:
(1)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:①CO(g)+2H2(g) CH3OH(g) △H1②CO2(g)+3H2(g)
CH3OH(g) △H1②CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H2 ③CO2(g) + H2(g)
CH3OH(g)+H2O(g) △H2 ③CO2(g) + H2(g)  CO(g)+H2O(g) △H3已知反应①中相关的化学键键能数据如下:
CO(g)+H2O(g) △H3已知反应①中相关的化学键键能数据如下:
由此计算△H1=___________ kJ•mol-1;已知△H2= -58 kJ•mol-1,则△H3= ___________ kJ•mol-1。
(2)燃料电池是符合绿色化学理念的新型发电装置,CH3OH—空气燃料电池是一种碱性(20%—30%的KOH溶液)燃料电池。电池放电时,负极的电极反应式为___________ 。正极的电极反应式为___________ 。
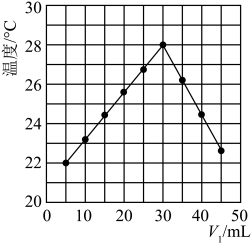
(3)将V1 mL 1.00 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是___________
(1)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:①CO(g)+2H2(g)
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1075 | 465 | 413 |
(2)燃料电池是符合绿色化学理念的新型发电装置,CH3OH—空气燃料电池是一种碱性(20%—30%的KOH溶液)燃料电池。电池放电时,负极的电极反应式为
(3)将V1 mL 1.00 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是___________

| A.做该实验时环境温度为22 ℃ |
| B.该实验表明化学能可以转化为热能 |
| C.NaOH溶液的浓度约为1.00 mol·L-1 |
| D.该实验表明有水生成的反应都是放热反应 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网