解答题-实验探究题 适中0.65 引用1 组卷188
苯甲酸又称安息香酸(C6H5COOH),可用于合成纤维、树脂涂料等也可作为药物或防腐剂使用,有抑制真菌、细菌生长的作用。实验室中由甲苯制备苯甲酸的实验如下:
查阅资料:
①苯甲酸是一元有机弱酸不易被氧化。在水中溶解度:0.35g(25℃)、2.7g(80℃)、5.9g(100℃)。甲苯易溶于有机溶剂,不溶于水。
②
实验步骤:
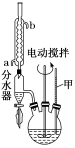
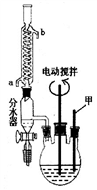
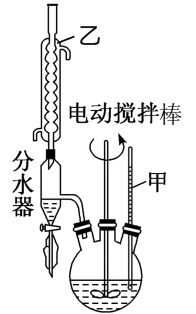
第一步:将9.2g甲苯和硫酸酸化的KMnO4溶液(过量)置于如图的三颈烧瓶中,加热保持反应物溶液温度在90℃左右至反应结束,主要反应为5C6H5CH3+6KMnO4+9H2SO4 5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
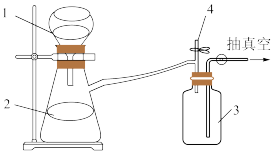
第二步:将反应后混合液趁热过滤滤液冷却后用硫酸酸化用如图装置抽滤得粗产品;(抽滤又称减压过滤利用抽气泵使抽滤瓶中的压强降低达到固液分离的目的。)
第三步:粗产品用水洗涤2到3次,干燥称量得固体 .
.
请回答下列问题:
(1)图1中装置乙的名称为___ 。
(2)分水器的作用是分离出水其主要目的是___ ,判断该反应进行完全的实验现象是___ 。
(3)实验第二步中,趁热过滤的原因是___ ,采用抽滤的优点是____ 。停止抽滤时先旋开图2中4处的旋塞恢复常压,然后关闭抽气泵,装置3起到的作用是____ 。
(4)第三步证明粗产品洗涤干净的方法是___ 。
(5)苯甲酸的产率为____ 。
(6)结合下列试剂和用品设计最简单实验验证苯甲酸是弱酸,具体操作为__ 。
0.010mol·L-1的苯甲酸溶液;0.010mol·L-1的苯甲酸钠溶液;0.010mol·L-1的氢氧化钠溶液;0.010mol·L-1的盐酸溶液;广泛pH试纸;甲基橙,酚酞(仪器任选)。
查阅资料:
①苯甲酸是一元有机弱酸不易被氧化。在水中溶解度:0.35g(25℃)、2.7g(80℃)、5.9g(100℃)。甲苯易溶于有机溶剂,不溶于水。
②
| 相对分子质量 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) | |
| 苯甲酸 | 122 | 122.4 | 249 | 1.3 |
| 甲苯 | 92 | -95 | 110.6 | 0.9 |
实验步骤:
第一步:将9.2g甲苯和硫酸酸化的KMnO4溶液(过量)置于如图的三颈烧瓶中,加热保持反应物溶液温度在90℃左右至反应结束,主要反应为5C6H5CH3+6KMnO4+9H2SO4

第二步:将反应后混合液趁热过滤滤液冷却后用硫酸酸化用如图装置抽滤得粗产品;(抽滤又称减压过滤利用抽气泵使抽滤瓶中的压强降低达到固液分离的目的。)

第三步:粗产品用水洗涤2到3次,干燥称量得固体
请回答下列问题:
(1)图1中装置乙的名称为
(2)分水器的作用是分离出水其主要目的是
(3)实验第二步中,趁热过滤的原因是
(4)第三步证明粗产品洗涤干净的方法是
(5)苯甲酸的产率为
(6)结合下列试剂和用品设计最简单实验验证苯甲酸是弱酸,具体操作为
0.010mol·L-1的苯甲酸溶液;0.010mol·L-1的苯甲酸钠溶液;0.010mol·L-1的氢氧化钠溶液;0.010mol·L-1的盐酸溶液;广泛pH试纸;甲基橙,酚酞(仪器任选)。
2020·内蒙古呼和浩特·二模
类题推荐
【小题1】苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:
 +KnMO4
+KnMO4
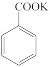 +MnO2
+MnO2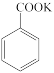 +HCl
+HCl
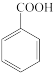 +KCl
+KCl
实验步骤:
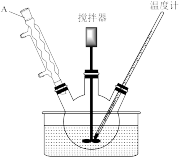
步骤1:在如图所示装置的三颈烧瓶中,加入1.5mL甲苯、100mL水和4.8g(约0.03mol)高锰酸钾,慢慢开启搅拌器,并加热至反应完全。
步骤2:停止加热,继续搅拌,冷却片刻后,慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣(MnO2)。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量___ 洗涤,放在沸水浴上干燥。称量,粗产品为1.0g。
步骤3:纯度测定:称取0.1220g粗产品,配成乙醇溶液,于100mL容量瓶中定容。每次移取25.00mL溶液,加入指示剂,用0.01000mol·L-1的KOH标准溶液滴定,三次滴定平均消耗22.30mL的KOH标准溶液。
回答下列问题:
(1)步骤1中,如图所示的装置中仪器A的名称是___________ ,作用是___________ 。
(2)加入适量饱和亚硫酸氢钠溶液的目的是(用离子方程式表示)___________ 。
(3)步骤2中,将析出的苯甲酸过滤,用少量___________ 洗涤。
(4)干燥苯甲酸晶体时,若温度过高,可能出现的结果是___________ 。
(5)步骤3中滴定时用的指示剂最好是___________。
(6)本实验制备的苯甲酸的纯度为____ (保留4位有效数字)
(7)若要得到纯度更高的苯甲酸,可通过在水中____ (填操作名称)的方法提纯。
 +KnMO4
+KnMO4 +MnO2
+MnO2 +HCl
+HCl +KCl
+KCl| 名称 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度(g·mL-1) | 溶解性 |
| 甲苯 | 92 | -95 | 110.6 | 0.867 | 不溶于水,易溶于乙醇 |
| 苯甲酸 | 122 | 122.4(100℃左右开始升华) | 248 | —— | 微溶于冷水,易溶于乙醇、热水 |
步骤1:在如图所示装置的三颈烧瓶中,加入1.5mL甲苯、100mL水和4.8g(约0.03mol)高锰酸钾,慢慢开启搅拌器,并加热至反应完全。

步骤2:停止加热,继续搅拌,冷却片刻后,慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣(MnO2)。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量
步骤3:纯度测定:称取0.1220g粗产品,配成乙醇溶液,于100mL容量瓶中定容。每次移取25.00mL溶液,加入指示剂,用0.01000mol·L-1的KOH标准溶液滴定,三次滴定平均消耗22.30mL的KOH标准溶液。
回答下列问题:
(1)步骤1中,如图所示的装置中仪器A的名称是
(2)加入适量饱和亚硫酸氢钠溶液的目的是(用离子方程式表示)
(3)步骤2中,将析出的苯甲酸过滤,用少量
(4)干燥苯甲酸晶体时,若温度过高,可能出现的结果是
(5)步骤3中滴定时用的指示剂最好是___________。
| A.石蕊试液 | B.酚酞试液 | C.甲基橙溶液 | D.淀粉溶液 |
(7)若要得到纯度更高的苯甲酸,可通过在水中
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网