解答题-实验探究题 适中0.65 引用1 组卷147
一种从乙醛工业中产生的废钯(Pd)催化剂(钯5-6%,炭93-94%,铁、铜、锌、镍1-2%)中提取PdCl2和CuCl2的工艺流程如图所示:
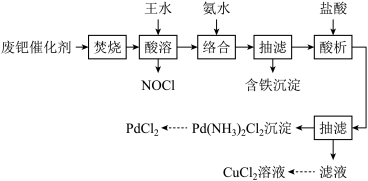
已知:钯、铜、锌、镍可与氨水形成Pd(NH3)42+等络离子。请回答:
(1)“焚烧”的主要目的为______________ ,实验室中可在______________ (填仪器名称)中模拟该过程。
(2)“酸溶”时,Pd转化为PdCl2,其化学方程式为______________ ;该过程需控温70-80℃,温度不能太低或太高的原因为______________ 。
(3)“络合”时,溶液的pH需始终维持8-9,则络合后溶液中含铁离子的浓度≦______________ 。(已知:Fe(OH)2、Fe(OH)3的Ksp甲分别为4×10-17、2.8×10-39)
(4)“酸析”时生成沉淀的离子方程式为______________ 。
(5)流程中回收得到的PdCl2和CuC12在乙烯直接氧化制乙醛的催化体系中联合发挥作用,反应机理如下:
i. ;
;
ii.______________;
iii. 。
。
ii的化学方程式为______________ 。
(6)上述提取PdCl2和CuCl2方案的缺点是______________ (写出一条即可)。

已知:钯、铜、锌、镍可与氨水形成Pd(NH3)42+等络离子。请回答:
(1)“焚烧”的主要目的为
(2)“酸溶”时,Pd转化为PdCl2,其化学方程式为
(3)“络合”时,溶液的pH需始终维持8-9,则络合后溶液中含铁离子的浓度≦
(4)“酸析”时生成沉淀的离子方程式为
(5)流程中回收得到的PdCl2和CuC12在乙烯直接氧化制乙醛的催化体系中联合发挥作用,反应机理如下:
i.
ii.______________;
iii.
ii的化学方程式为
(6)上述提取PdCl2和CuCl2方案的缺点是
19-20高三·河北石家庄·阶段练习
类题推荐
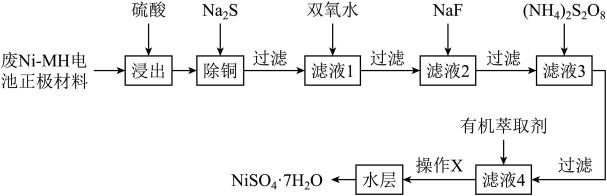
某科研人员以废镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO)为原料回收镍,工艺流程如图。

已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如表。
回答下列问题:
(1)浸出渣主要成分为_______ 、_______ 。(填化学式)
(2)“除铜”时,Fe3+与H2S反应的离子方程式为_______ 。
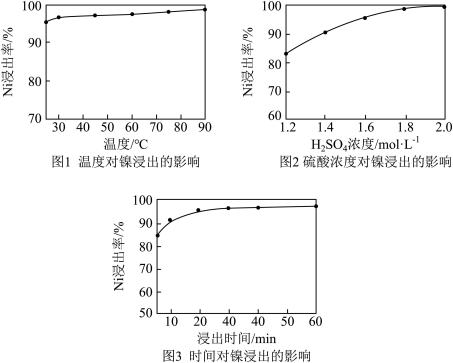
(3)“氧化”的目的是将溶液中Fe2+氧化为Fe3+,温度需控制在40~50℃之间,该步骤温度不能太高的原因是_______ 。
(4)“调pH”时,pH的控制范围为_______ 。
(5)“除钙”后,若溶液中F-浓度为3×10-3mol•L-1,则 =
=_______ 。[已知常温下,Ksp(CaF2)=2.7×10-11]
(6)常温下,Ksp[Fe(OH)3]=1×10-38,要使溶液中的Fe3+沉淀完全[残留在溶液中的c(Fe3+)<10-5mol•L-1],则溶液的pH应大于_______ 。
(7)用可溶性碳酸盐,可以浸取CaSO4固体,在溶液浸取过程中会发生反应:CaSO4(s)+ (ag)⇌CaCO3(s)+
(ag)⇌CaCO3(s)+ (aq)。已知:298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为
(aq)。已知:298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为_______ (计算结果保留三位有效数字)。

已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如表。
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
回答下列问题:
(1)浸出渣主要成分为
(2)“除铜”时,Fe3+与H2S反应的离子方程式为
(3)“氧化”的目的是将溶液中Fe2+氧化为Fe3+,温度需控制在40~50℃之间,该步骤温度不能太高的原因是
(4)“调pH”时,pH的控制范围为
(5)“除钙”后,若溶液中F-浓度为3×10-3mol•L-1,则
(6)常温下,Ksp[Fe(OH)3]=1×10-38,要使溶液中的Fe3+沉淀完全[残留在溶液中的c(Fe3+)<10-5mol•L-1],则溶液的pH应大于
(7)用可溶性碳酸盐,可以浸取CaSO4固体,在溶液浸取过程中会发生反应:CaSO4(s)+
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网