解答题-原理综合题 适中0.65 引用1 组卷91
近年来甲醇用途日益广泛,工业上甲醇的合成途径多种多样。现有实验室中模拟甲醇合成反应,在2L密闭刚性的容器内,加入物质的量之比为 的
的 和
和 ,400℃时反应:
,400℃时反应:
体系中 随时间的变化如下表:
随时间的变化如下表:
(1)用 表示从0~2s内该反应的平均速率
表示从0~2s内该反应的平均速率
_______________ 。
(2)能说明该反应已达到平衡状态的是_______________ 。
a. b.容器内压强保持不变
b.容器内压强保持不变
c. d.容器内密度保持不变
d.容器内密度保持不变
(3)达到平衡时,甲醇在平衡体系中的体积分数为__________ (保留小数点后一位)。
(4) 与
与 的反应可将化学能转化为电能,若用硫酸做电解质溶液形成原电池,
的反应可将化学能转化为电能,若用硫酸做电解质溶液形成原电池, 应通入电池的
应通入电池的_________ 极(“正”、“负”),且正极的电极反应式为_____________ 。
体系中
| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |
(1)用
(2)能说明该反应已达到平衡状态的是
a.
c.
(3)达到平衡时,甲醇在平衡体系中的体积分数为
(4)
19-20高一下·河南郑州·阶段练习
类题推荐
近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。现有实验室中模拟甲醇的合成反应,在2L密闭容器内,400℃时反应: ,体系中
,体系中 随时间的变化如表:
随时间的变化如表:
根据图表回答下列问题:
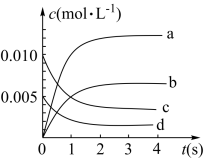
(1)图中表示 的变化的曲线是
的变化的曲线是___________ 。
(2)用 表示从0~2s内该反应的平均速率
表示从0~2s内该反应的平均速率
___________ 。
(3)能说明该反应已达到平衡状态的是___________ 。
a. b.容器内压强保持不变
b.容器内压强保持不变
c.生成 的同时消耗
的同时消耗 d.容器内密度保持不变
d.容器内密度保持不变
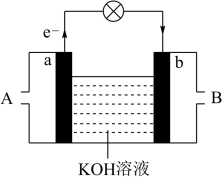
(4)已知 与
与 的反应可将化学能转化为电能,其工作原理如图所示,图中
的反应可将化学能转化为电能,其工作原理如图所示,图中 从
从___________ (填A或B)通入,a极的电极反应式是___________ 。
| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |
(1)图中表示

(2)用
(3)能说明该反应已达到平衡状态的是
a.
c.生成
(4)已知

近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。现有实验室中模拟甲醇合成反应,在2L密闭容器内以物质的量比2:3充入CO和H2,400℃时反应:CO(g)+2H2(g) CH3OH(g),体系中n(CO)随时间的变化如表:
CH3OH(g),体系中n(CO)随时间的变化如表:
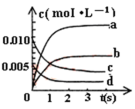
(1)如图表示反应中CH3OH的变化曲线,其中合理的是___________ 。
(2)用CO表示从0~2s内该反应的平均速率v(CO)=___________ 。
(3)能说明该反应已达到平衡状态的是___________ 。
a.v(CH3OH)=2v(H2)
b.容器内压强保持不变
c.断开2molH-H键的同时断开4molC-H键
d.容器内密度保持不变
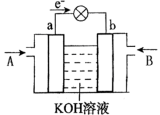
(4)CH3OH与O2的反应可将化学能转化为电能,其工作原理如图所示,图中CH3OH从___________ (填A或B)通入,a极附近溶液pH将___________ (填升高,降低或不变),b极的电极反应式是___________ 。
| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |

(1)如图表示反应中CH3OH的变化曲线,其中合理的是
(2)用CO表示从0~2s内该反应的平均速率v(CO)=
(3)能说明该反应已达到平衡状态的是
a.v(CH3OH)=2v(H2)
b.容器内压强保持不变
c.断开2molH-H键的同时断开4molC-H键
d.容器内密度保持不变
(4)CH3OH与O2的反应可将化学能转化为电能,其工作原理如图所示,图中CH3OH从

近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。现有实验室中模拟甲醇合成反应,在2L密闭容器内,400℃时反应:CO(g)+2H2(g) CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:
CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:
(1)图中表示CH3OH的变化的曲线是____ 。
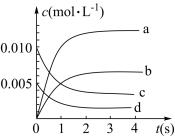
(2)用H2表示从0~2s内该反应的平均速率v(H2)=____ 。
(3)能说明该反应已达到平衡状态的是___ 。
a.反应中CO与CH3OH的物质的量之比为1:1
b.容器内压强保持不变
c.2v逆(CO)=v正(H2)
d.单位时间内每消耗1molCO,同时生成1molCH3OH
(4)CH3OH与O2的反应可将化学能转化为电能,工作原理如图所示,则CH3OH应从____ (填A或B)通入,K+移向____ (填a、b极),当电路中累计有2mol电子通过时,消耗的氧气体积为(在标准状况下)____ L。
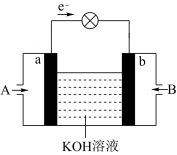
(5)通CH3OH的一极的电极反应式为____ 。
| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |
(1)图中表示CH3OH的变化的曲线是

(2)用H2表示从0~2s内该反应的平均速率v(H2)=
(3)能说明该反应已达到平衡状态的是
a.反应中CO与CH3OH的物质的量之比为1:1
b.容器内压强保持不变
c.2v逆(CO)=v正(H2)
d.单位时间内每消耗1molCO,同时生成1molCH3OH
(4)CH3OH与O2的反应可将化学能转化为电能,工作原理如图所示,则CH3OH应从

(5)通CH3OH的一极的电极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


