填空题 适中0.65 引用1 组卷77
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.Zn+H2SO4=ZnSO4+H2↑;B.NaOH+HCl=NaCl+H2O。能设计成原电池的反应是__________ (填“A”或“B”)。
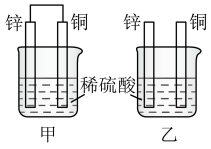
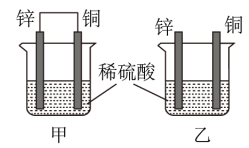
(2)将锌片和铜片按如图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
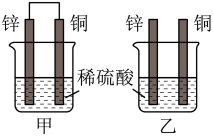
①下列说法正确的是__________ 。
A.甲、乙均为化学能转变为电能的装置
B.甲中铜片质量减少、乙中锌片质量减少
C.两烧杯中溶液的c(H+)均减小
②在相同时间内,两烧杯中产生气泡的速度:甲__________ 乙(填“>”、“<”或“=”)。
③请写出图中构成原电池的正极电极反应式:__________ 。
④当乙中产生2.24 L(标准状况)气体时,将锌铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.2 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为__________ 。
(1)现有如下两个反应:A.Zn+H2SO4=ZnSO4+H2↑;B.NaOH+HCl=NaCl+H2O。能设计成原电池的反应是
(2)将锌片和铜片按如图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置
B.甲中铜片质量减少、乙中锌片质量减少
C.两烧杯中溶液的c(H+)均减小
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的正极电极反应式:
④当乙中产生2.24 L(标准状况)气体时,将锌铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.2 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为
19-20高一下·湖南郴州·阶段练习
类题推荐
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:
A:NaOH+HCl=NaCl+H2O;
B:Zn+H2SO4=ZnSO4+H2↑
判断能否设计成原电池A______ ,B ______ (填“能”或“不能”)。
将纯锌片和纯铜片按图方式插入 相同浓度的稀硫酸中一段时间,回答下列问题:
相同浓度的稀硫酸中一段时间,回答下列问题:
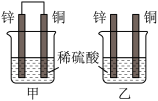
(2)下列说法正确的是_____________。
(3)在相同时间内,两烧杯中产生气泡的速度:甲___________ 乙 填“
填“ ”、“
”、“ “或“
“或“ ”
”
(4)请写出图中构成原电池的负极电极反应式_____________________ 。电池工作时,溶液中 向
向_______ 极移动电池工作完成后,溶液中 浓度
浓度__________  填增大或减小或不变
填增大或减小或不变 。
。
(5)若正极析出氢气的质量为3.2g,则电路中转移_______ 个电子。
(1)现有如下两个反应:
A:NaOH+HCl=NaCl+H2O;
B:Zn+H2SO4=ZnSO4+H2↑
判断能否设计成原电池A
将纯锌片和纯铜片按图方式插入

(2)下列说法正确的是_____________。
| A.甲、乙均为化学能转变为电能的装置 |
| B.乙中铜片上没有明显变化 |
| C.甲中铜片质量减少、乙中锌片质量减少 |
| D.两烧杯中溶液中的H+均减小 |
(4)请写出图中构成原电池的负极电极反应式
(5)若正极析出氢气的质量为3.2g,则电路中转移
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网